03/08/2023
Proteiner er livets byggesten, og at kende deres størrelse er afgørende for at forstå deres funktioner. En af de mest udbredte og effektive teknikker til at bestemme proteiners molekylvægt og kvantitet er SDS-polyacrylamid gel-elektroforese, bedre kendt som SDS-PAGE. Denne metode er designet til at adskille proteiner udelukkende baseret på deres størrelse, uafhængigt af andre fysiske egenskaber.
- Forståelsen bag SDS-PAGE
- Relativ Mobilitet og Molekylvægt
- Trin for Trin Proces: Fremstilling og Kørsel af SDS-PAGE Gel
- Resultater og Beregninger
- Diskussion af SDS-PAGE Principper og Anvendelser
- Hvordan Bestemmes Relativ Mobilitet i Gel-elektroforese?
- Bestemmelse af Molekylvægt med Gradient SDS Geler
- Ofte Stillede Spørgsmål om SDS-PAGE
- Hvorfor bruges SDS i SDS-PAGE?
- Hvad er forskellen mellem en stacking gel og en separationsgel?
- Hvorfor er det vigtigt at tilsætte TEMED sidst?
- Hvordan påvirker gelens porestørrelse proteinseparationen?
- Hvad er formålet med Coomassie Brilliant Blue-farvning?
- Hvad er nøjagtigheden af molekylvægtsbestemmelse med SDS-PAGE?
Forståelsen bag SDS-PAGE
SDS-PAGE er en kraftfuld teknik, der bygger på principperne om elektrisk ladning og et filtrerende gel-matrix. Kernen i metoden er brugen af natriumdodecylsulfat (SDS), et anionisk detergent. Når SDS opløses, får dets molekyler en netonegativ ladning over et bredt pH-område. En polypeptidkæde binder en mængde SDS, der er proportional med dens relative molekylmasse. De negative ladninger fra SDS ødelægger det meste af proteinernes komplekse struktur, hvilket denaturerer dem og gør dem til lineære kæder. Disse SDS-belagte polypeptider trækkes derefter stærkt mod en anode (positivt ladet elektrode) i et elektrisk felt.
Samtidig fungerer polyacrylamidgeler som et molekylært si. De begrænser større molekyler fra at migrere lige så hurtigt som mindre molekyler. Fordi forholdet mellem ladning og masse er næsten det samme blandt SDS-denaturerede polypeptider – takket være SDS'ens evne til at give alle proteiner en ensartet negativ ladning i forhold til deres masse – afhænger den endelige adskillelse af proteiner næsten udelukkende af forskellene i polypeptidets relative molekylmasse. Dette gør SDS-PAGE til en ideel metode til at bestemme proteiners størrelse.
Relativ Mobilitet og Molekylvægt
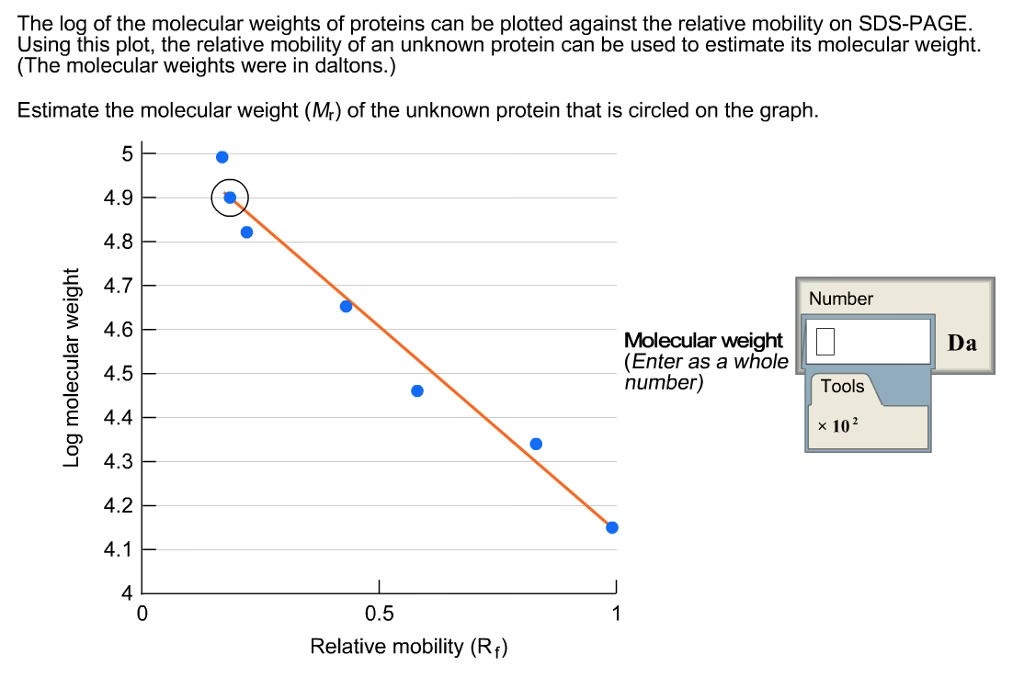
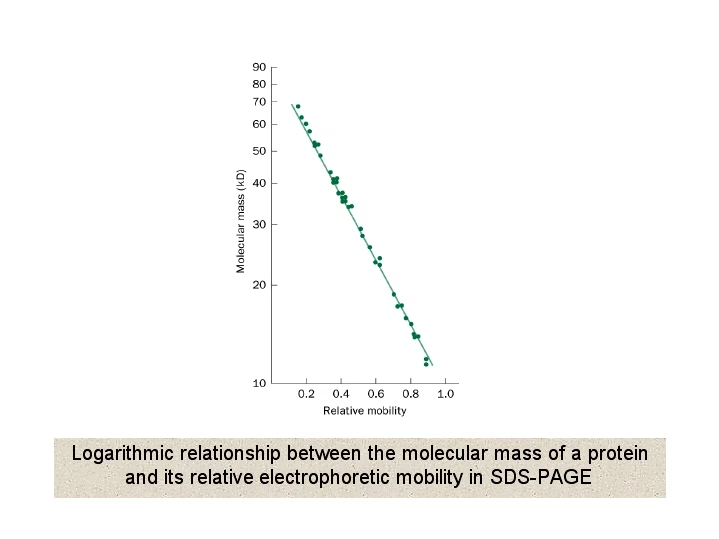
I en gel med ensartet tæthed er et proteins relative migrationsafstand negativt proportional med logaritmen af dets masse. Hvis proteiner med kendt masse (molekylvægtsstandarder) køres samtidigt med ukendte proteiner, kan forholdet mellem relativ mobilitet og masse plottes. Dette skaber en standardkurve, der gør det muligt at estimere massen af de ukendte proteiner. Nøglen til nøjagtig molekylvægtsbestemmelse er at vælge separationsbetingelser, der producerer et lineært forhold mellem logaritmen af molekylvægten (log MW) og migration inden for det sandsynlige MW-område for det ukendte protein.
Efter separationen skal den relative migrationsafstand (Rf) for proteinstandarderne og det ukendte protein bestemmes. Rf defineres som proteinets mobilitet divideret med ionfrontens mobilitet. Da ionfronten kan være svær at lokalisere, normaliseres mobiliteterne til en tracking dye, der migrerer lige bag ionfronten:
Rf = (afstand til bånd) / (afstand til farvefront)
Ved at bruge de værdier, der er opnået for proteinstandarderne, vil en graf over log MW kontra Rf være lineær for de fleste proteiner, forudsat at de er fuldt denatureret, og at gelprocenten er passende for prøvens MW-område. Standardkurven er sigmoidal ved ekstreme MW-værdier, fordi ved høj MW er si-effekten af matricen så stor, at molekylerne ikke kan trænge ind i gelen; ved lav MW er si-effekten ubetydelig, og proteiner migrerer næsten frit. Nøjagtigheden af MW-estimering med SDS-PAGE ligger typisk i området 5-10%.
Trin for Trin Proces: Fremstilling og Kørsel af SDS-PAGE Gel
Processen med at udføre SDS-PAGE involverer omhyggelig forberedelse af gelerne og prøverne samt præcis udførelse af elektroforesen. Her er en detaljeret beskrivelse af den typiske metodologi:
Gel Forberedelse
Først fremstilles en stamopløsning af acrylamid ved at blande 3,00 g acrylamid med 0,08 g methylen-bis-acrylamid og 10,0 ml dobbelt destilleret vand. Denne opløsning opbevares ved +4°C. Separationsgelen, som er ansvarlig for den primære separation baseret på størrelse, fremstilles ved at tilsætte 2,00 ml acrylamid-stamopløsning, 2,24 ml Tris pH 8,8 (fremstillet ved blanding af 6,05 g Tris, 0,94 ml HCl og 49,96 ml destilleret vand), 1,74 ml destilleret vand, 30,0 µl 10% SDS (fremstillet ved blanding af 2,00 g natriumdodecylsulfat og 20,0 ml destilleret vand, kan opbevares ved stuetemperatur), 4,00 µl Tetramethylethylendiamin (TEMED) og 20,0 µl 10% ammoniumpersulfat (fremstillet ved at tilsætte 0,10 g ammoniumpersulfat til 1,0 ml destilleret vand). Det er vigtigt at bemærke, at TEMED tilsættes sidst, da det initierer polymerisationen.
Gel Støbning
De korte og afstandsplader (Bio-Rad, Mini-PROTEANTM) vaskes grundigt med destilleret vand, behandles derefter med 70% alkohol og lufttørres. Efter at have placeret den korte plade oven på afstandspladen, forsegles bunden og siderne med Parafilm®. På en plan overflade skydes de to plader ind i støberammen med den korte plade vendt fremad. Trykklemmerne låses for at sikre glaspladerne. Støberammen fastgøres i støbestativet ved at forbinde den fjederbelastede arm. Afstandspladen skubbes ned mod den grå gummipakning af armen, og separationsgelen støbes op til tre fjerdedele af pladens højde.
Efter støbning hældes butanol oven på geloverfladen for at forhindre gelens fordampning og for at udjævne geloverfladen. Gelen stivner i cirka en halv time ved stuetemperatur. Derefter hældes butanolen fra, og geloverfladen skylles med destilleret vand.
Stacking Gel Forberedelse og Støbning
En stacking gel fremstilles ved at tilsætte 0,835 ml acrylamid-stamopløsning, 0,625 ml Tris pH 8,8, 3,515 ml destilleret vand, 50,0 µl 10% SDS, 5,00 µl TEMED og 25,0 µl 10% ammoniumpersulfat. Igen tilsættes TEMED sidst.
Stacking gelen støbes derefter ovenpå separationsgelen, og en kam indsættes for at danne brønde til prøveladning. Dette efterlades i 30 minutter ved stuetemperatur for at stivne. Gelkassetten fjernes derefter fra støberammen.
Prøve Forberedelse og Kørsel
Gelkassetten placeres i elektrodeopsætningen med den korte plade vendt indad. Gelkassetterne og elektrodeopsætningen skydes ind i klemmerammen. Elektrodeopsætningen trykkes ned, mens de to kamhåndtag på klemmerammen lukkes. Derefter sænkes det indre kammer ned i minitanken. Løbebufferen hældes derefter på apparatet og nedsænker det fuldstændigt. Kammen fjernes forsigtigt.
Før ladning opvarmes 2 µl flagermusserumprøver ved 100°C i 2-5 minutter i en prøvebuffer-cocktail med tilsætning af 5% 2-mercaptoethanol. Denne opvarmning og tilsætning af reduktionsmiddel sikrer fuldstændig denaturering af proteinerne og bryder disulfidbindinger. De behandlede prøver indlæses i brøndene. Gelen køres på Bio-Rad Power-Pac 1000 med en konstant strøm på 20 mA/gel under stacking-fasen og 40 mA/gel under separationsfasen.
Farvning og Affarvning
Efter kørslen tages gelen forsigtigt ud af minitanken, elektrodeopsætningen og gelkassetten og placeres på en plan overflade. Stacking-gelkomponenten fjernes med en plastikskraber, og den resterende separationsgel nedsænkes i Coomassie brilliant blue-farveopløsning (0,25 g Coomassie brilliant blue, 112,5 ml methanol, 112,5 ml dobbelt destilleret vand, 25,0 ml glacial eddikesyre). Farveopløsningen filtreres gennem Whatman No: 1 papir. Gelen farves i en time på en rystemaskine ved ca. 28 omdrejninger pr. minut. Derefter fjernes farven, og gelen nedsænkes i affarvningsopløsning på rystemaskinen. Affarvningsopløsningen udskiftes hvert 10-15 minut, indtil baggrundsfarven er ubetydelig, og båndfarvningen er klar.
Resultater og Beregninger
Efter farvning og affarvning måles afstanden til farvefronten og de enkelte proteinbånd. I dette eksperiment blev farvefronten målt til 4,4 cm.
Relative Mobiliteter
Den relative mobilitet (Rf) beregnes for både markørproteinerne (med kendt molekylvægt) og proteinerne i flagermusserummet. Formlen er simpelthen afstanden, båndet har tilbagelagt, divideret med afstanden, farvefronten har tilbagelagt.
Markør:
- 1. bånd: 0,4 cm / 4,4 cm = 0,091
- 2. bånd: 0,8 cm / 4,4 cm = 0,182
- 3. bånd: 1,6 cm / 4,4 cm = 0,364
- 4. bånd: 2,4 cm / 4,4 cm = 0,545
- 5. bånd: 2,8 cm / 4,4 cm = 0,636
- 6. bånd: 3,1 cm / 4,4 cm = 0,705
- 7. bånd: 3,4 cm / 4,4 cm = 0,773
- 8. bånd: 3,8 cm / 4,4 cm = 0,864
- 9. bånd: 4,4 cm / 4,4 cm = 1,000
Flagermusserum:
- 1. bånd: 0,4 cm / 4,4 cm = 0,091
- 2. bånd: 1,0 cm / 4,4 cm = 0,227
- 3. bånd: 1,2 cm / 4,4 cm = 0,273
- 4. bånd: 1,6 cm / 4,4 cm = 0,364
- 5. bånd: 2,0 cm / 4,4 cm = 0,455
- 6. bånd: 2,75 cm / 4,4 cm = 0,625
- 7. bånd: 3,25 cm / 4,4 cm = 0,739
- 8. bånd: 3,35 cm / 4,4 cm = 0,761
- 9. bånd: 3,55 cm / 4,4 cm = 0,807
Tabel 1: Molekylvægt vs. Relativ Mobilitet (Markør)
| Relativ mobilitet | Molekylvægt (kDa) |
|---|---|
| 0,091 | 220 |
| 0,182 | 150 |
| 0,364 | 75 |
| 0,545 | 50 |
| 0,636 | 32 |
| 0,705 | 25 |
| 0,773 | 15 |
| 0,864 | 6 |
Baseret på en graf over logaritmen af molekylvægten (y-akse) mod den relative mobilitet (x-akse) fra markørproteinerne, opnås en ligning for standardkurven. I dette tilfælde er ligningen angivet som: y = -222,4x + 202,3. Denne ligning bruges til at beregne molekylvægten af de ukendte proteiner i flagermusserummet ved at indsætte deres målte relative mobiliteter som 'x'.
Tabel 2: Molekylvægt af båndene i flagermusserummet
| Relativ mobilitet | Molekylvægt (kDa) |
|---|---|
| 0,091 | 182,0616 |
| 0,227 | 151,8152 |
| 0,273 | 141,5848 |
| 0,364 | 121,3464 |
| 0,455 | 101,108 |
| 0,625 | 63,3 |
| 0,739 | 37,9464 |
| 0,761 | 33,0536 |
Diskussion af SDS-PAGE Principper og Anvendelser
Polyacrylamidgel er et syntetisk, termostabilt, gennemsigtigt, stærkt og kemisk relativt inert gel, der kan fremstilles med et bredt spektrum af gennemsnitlige porestørrelser. Pore størrelsen af en gel bestemmes af to faktorer: den samlede mængde acrylamid, der er til stede, og mængden af tværbinder. Det er afgørende at udvise forsigtighed ved håndtering af acrylamid, da det er ekstremt toksisk og kan forårsage lammelse af centralnervesystemet. Hvor agarosegeler er bedst til at køre større molekyler som DNA, er SDS-PAGE bedre egnet til mindre molekyler som proteiner.
SDS-PAGE har en række anvendelsesmuligheder, herunder:
- Fastlæggelse af proteinstørrelse
- Proteinidentifikation
- Bestemmelse af prøverens renhed
- Identifikation af disulfidbindinger
- Kvantificering af proteiner
- Blotting-applikationer (f.eks. Western blot)
Den Discontinue Buffersystem og SDS's Rolle
Hastigheden af en ladet partikel, der bevæger sig i et elektrisk felt, er direkte proportional med feltstyrken og molekylets ladning og omvendt proportional med molekylets størrelse og mediets viskositet. For at øge opløsningen af proteinseparation under SDS-polyacrylamid gel-elektroforese anvendes ofte et discontinu buffersystem. To gellag blev fremstillet i pladen: en stacking gel og en separationsgel. Stacking gelen indeholder kloridioner, de ledende ioner, som migrerer hurtigere gennem gelen end proteinprøven, mens elektroforesebufferen (Tris-buffer) indeholder glycinioner, de efterfølgende ioner, som migrerer langsommere. Proteinmolekylerne fanges i et skarpt bånd mellem disse ioner. Når proteinet trænger ind i separationsgelen, som har en mindre porestørrelse, en højere pH og en højere saltkoncentration, ioniseres glycinen, spændingsgradienten forsvinder, og proteinet adskilles baseret på størrelse.
SDS er et ionisk detergent, der binder sig til langt de fleste proteiner i et konstant forhold på 1,4 g SDS pr. gram protein. SDS er et stærkt denatureringsmiddel, der bruges til at denaturere native proteiner til udfoldede, individuelle polypeptider. Da SDS er et anionisk detergent, giver det en negativ ladning til alle proteiner i prøven. Endnu vigtigere er det, at disse ladninger oversvømmer proteinernes iboende ladning og giver hvert protein det samme ladnings-til-masse-forhold. Få proteiner som tubulin binder ikke i dette forhold, og dette er en grund til, at nogle proteiner migrerer anomaløst. Fordi proteinerne har det samme ladnings-til-masse-forhold, og fordi gelerne har si-egenskaber, bliver mobiliteten en funktion af molekylvægten.
Kemiske Tilsætningsstoffer: TEMED, Ammoniumpersulfat og Coomassie Brilliant Blue
TEMED (N, N, N', N'-tetramethylethylendiamin) (C6H16N2; MW: 116,21) stabiliserer frie radikaler og forbedrer polymerisationen. Polymerisationshastigheden og egenskaberne af den resulterende gel afhænger af koncentrationen af frie radikaler. Øget mængde af frie radikaler resulterer i en reduktion af den gennemsnitlige polymerkædelængde og gelens elasticitet, men det øger gelens turbiditet. TEMED skal opbevares i køleskabet i mørke glasflasker, og det tilsættes sidst, da det starter polymerisationen og får polyacrylamid til at stivne.
Ammoniumpersulfat er også en kilde til frie radikaler og bruges ofte som en initiator for gelformation. Ammoniumpersulfat bør fremstilles frisk eller bruges fra et relativt frisk lager, da det mister sin effektivitet efter en uge eller to i køleskabet.
Coomassie Brilliant Blue er den mest populære proteinfarve. Det er et anionisk farvestof, der ikke-specifikt binder sig til proteiner. Overskydende farvestof, der er indarbejdet i gelen, kan fjernes ved affarvning med den samme opløsning uden farvestof. Proteinerne detekteres som blå bånd på en klar baggrund. Da SDS også er anionisk, kan det interferere med farvningsprocessen. Derfor anbefales et stort volumen farveopløsning, mindst ti gange gelens volumen.
Når data fra standardmarkøren plottes (log molekylvægt mod relativ mobilitet), kan vi opnå en standardkurve og en ligning. Ved at bruge denne ligning kan vi derefter bestemme molekylvægten af proteinerne i flagermusserummet eller andre ukendte prøver.
Hvordan Bestemmes Relativ Mobilitet i Gel-elektroforese?
Mobiliteten (Rf) af et molekyle i gel-elektroforese bestemmes af dets frie opløsningsmobilitet, Y0 (mobilitet i en gel med nul procent), og gelmatrixens si-virkning. I denaturerende proteindlektroforese, hvor SDS tilsættes elektroforesebufferen, dækkes proteinerne ensartet med negative ladninger. Dette udligner ladnings-til-masse-forholdet for alle proteiner, hvilket gør Y0 den samme for alle arter. I dette tilfælde bestemmes relative mobiliteter udelukkende af gelens si-virkning. Denne si-virkning er proportional med molekylvægten (MW) af det pågældende protein. Teoretiske behandlinger antyder, at logaritmen af Rf bør variere med MW, men de fleste brugere anvender en empirisk plot af logaritmen af MW mod Rf for flere standarder med kendte molekylvægte for at bestemme molekylvægten af ukendte proteiner.
I praksis holder proportionaliteten af log(MW) vs. Rf for de fleste proteiner, forudsat at de er fuldt denatureret, og at gelprocenten er valgt til at matche prøvens molekylvægtsområde. Faktisk er den faktiske graf af log(MW) vs. Rf sigmoidal, fordi ved høj MW er si-effekten af matrixen så stor, at molekyler ikke kan trænge ind i gelen, mens ved lav MW er si-effekten ubetydelig, og proteiner migrerer næsten med deres frie mobilitet, som i SDS er uafhængig af MW.
Givet et passende valg af gelprocent og et protein, der udviser næsten ideel adfærd, kan molekylvægten bestemmes med en nøjagtighed på 5-10%. Molekylvægten af ikke-ideelle proteiner kan bestemmes ved brug af Ferguson-plots, en teknik der anvender native protein-elektroforese.
Bestemmelse af Molekylvægt med Gradient SDS Geler
Hvis der introduceres en acrylamidkoncentrationsgradient i SDS-PAGE, kan større områder af proteiner analyseres på de samme geler med større opløsning. Kompleksiteten af forholdet mellem migration og molekylvægt afhænger af gradientens form. Den overordnede ligning er af formen log(MW) α log(P), hvor P er koncentrationen af acrylamid ved båndpositionen. En graf af log(MW) vs. log(P) er lineær og gør det muligt at bestemme MW'er ud fra et sæt standardproteinpositioner. For lineære gradientgeler er procentdelen af acrylamid proportional med positionen i gelen, så log(MW) vil være proportional med log(båndposition). Derfor vil en graf af log(MW) vs. log(Rf) for et sæt standarder være lineær, og Rf-værdier for ukendte kan derefter konverteres til MW-værdier. På en 3-30% gradientgel kan et område af proteiner, der adskiller sig i MW med op til 100 gange, opløses, og MW'er bestemmes.
Ofte Stillede Spørgsmål om SDS-PAGE
Her er nogle af de mest almindelige spørgsmål vedrørende SDS-PAGE-teknikken:
Hvorfor bruges SDS i SDS-PAGE?
SDS (natriumdodecylsulfat) er et anionisk detergent, der denaturerer proteiner og giver dem en ensartet negativ ladning i forhold til deres masse. Dette sikrer, at proteinerne udelukkende adskilles baseret på deres størrelse, da deres ladnings-til-masse-forhold bliver ens.
Hvad er forskellen mellem en stacking gel og en separationsgel?
Stacking gelen har en lavere acrylamidkoncentration og pH, hvilket tillader proteiner at 'stacke' (samles) i et skarpt bånd, før de trænger ind i separationsgelen. Separationsgelen har en højere acrylamidkoncentration og pH, hvilket skaber en finere porestørrelse, der adskiller proteinerne baseret på deres molekylvægt.
Hvorfor er det vigtigt at tilsætte TEMED sidst?
TEMED (Tetramethylethylendiamin) er en katalysator, der initierer polymerisationen af acrylamid. Hvis det tilsættes for tidligt, vil gelen begynde at stivne, før alle komponenter er blandet korrekt, eller før gelen er støbt.
Hvordan påvirker gelens porestørrelse proteinseparationen?
Gelens porestørrelse bestemmes af koncentrationen af acrylamid og tværbinderen. En mindre porestørrelse (højere acrylamidkoncentration) giver bedre separation af mindre proteiner, mens en større porestørrelse (lavere acrylamidkoncentration) er bedre til større proteiner. Valg af den rigtige gelprocent er afgørende for optimal opløsning af proteiner inden for et specifikt molekylvægtsområde.
Hvad er formålet med Coomassie Brilliant Blue-farvning?
Coomassie Brilliant Blue er et farvestof, der binder sig non-specifikt til proteiner, hvilket gør dem synlige som blå bånd på gelen. Dette giver forskere mulighed for at visualisere de adskilte proteiner og analysere deres tilstedeværelse, størrelse og relative mængde.
Hvad er nøjagtigheden af molekylvægtsbestemmelse med SDS-PAGE?
Nøjagtigheden af molekylvægtsestimering med SDS-PAGE ligger typisk i området 5-10%, forudsat at proteinerne er fuldt denatureret, og at gelprocenten er passende for prøvens molekylvægtsområde.
Hvis du vil læse andre artikler, der ligner Proteinstørrelse: SDS-PAGE og Relativ Mobilitet, kan du besøge kategorien Mobil.