06/05/2023
I biokemi, cellebiologi og immunologi er evnen til at analysere proteiner efter størrelse afgørende. En af de mest udbredte og citerede metoder til dette formål er SDS-PAGE (natriumdodecylsulfat-polyacrylamidgel-elektroforese). Denne teknik har revolutioneret vores forståelse af proteiner, idet den muliggør hurtig og omkostningseffektiv separation af selv de mindste proteinmængder fra vævs- og celleekstrakter. Mens molekylvægten af vandopløselige proteiner pålideligt kan bestemmes ud fra deres mobilitet på en SDS-PAGE-gel, har forskere i årtier stået over for en uforudsigelig udfordring: hvordan helikale membranproteiner migrerer. Disse proteiner, som udgør 20-30% af genomer og størstedelen af lægemiddelmål, bevæger sig ofte til positioner, der er enten langsommere eller hurtigere, end deres faktiske molekylvægt tilsiger. Denne 'anomale migration' har længe forvirret forskere og kompliceret proteinidentifikation. Men ny forskning har nu afsløret, at omfanget og retningen af denne migration blandt membranproteinmimetika kontrolleres af akrylamidkoncentrationen i gelen, hvilket åbner døren for en mere ligetil analyse af disse vitale biomolekyler.
Grundlæggende om SDS-PAGE: Hvordan fungerer proteinseparation?
SDS-PAGE-systemet, oprindeligt udviklet af Laemmli, er et kraftfuldt analytisk værktøj til at studere proteinmolekyler. Processen er relativt simpel, overkommelig og hurtig. Først blandes proteinprøven med en buffer, der indeholder sporfarve og detergentet SDS. SDS (natriumdodecylsulfat) er et anionisk detergent, der denaturerer proteiner, dvs. folder dem ud til lineære kæder. Samtidig binder SDS sig til proteinerne i et forholdsvis konstant forhold (ca. 1,4 gram SDS pr. gram protein), hvilket giver protein-SDS-komplekset en ensartet negativ ladning i forhold til dets masse. Dette er afgørende, da det sikrer, at proteinernes mobilitet primært afhænger af deres størrelse og ikke deres iboende ladning eller oprindelige tredimensionelle struktur.
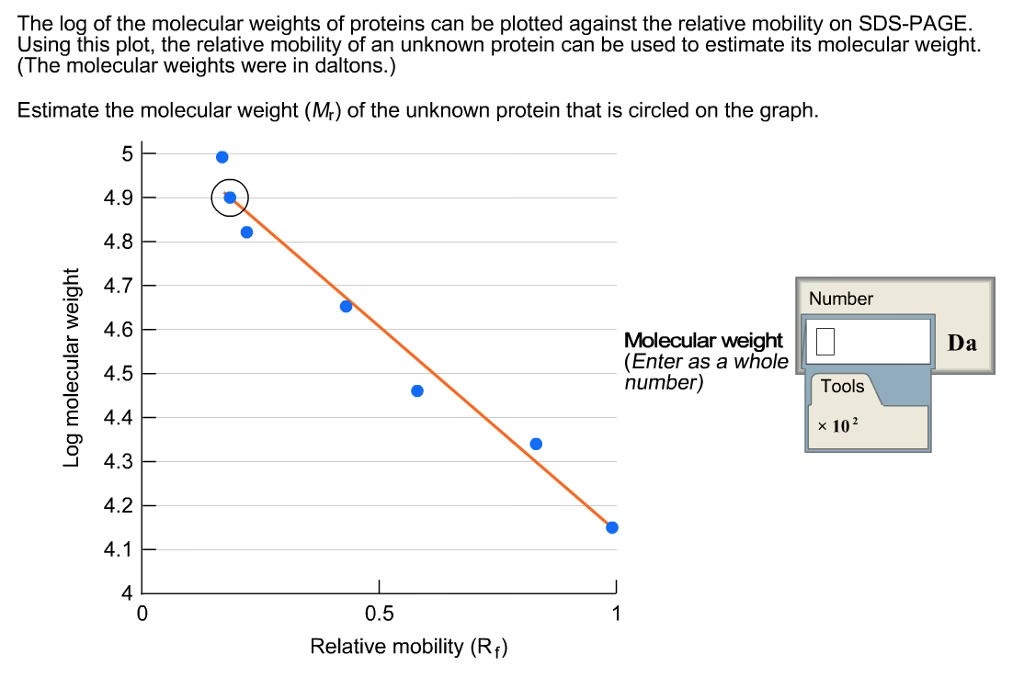
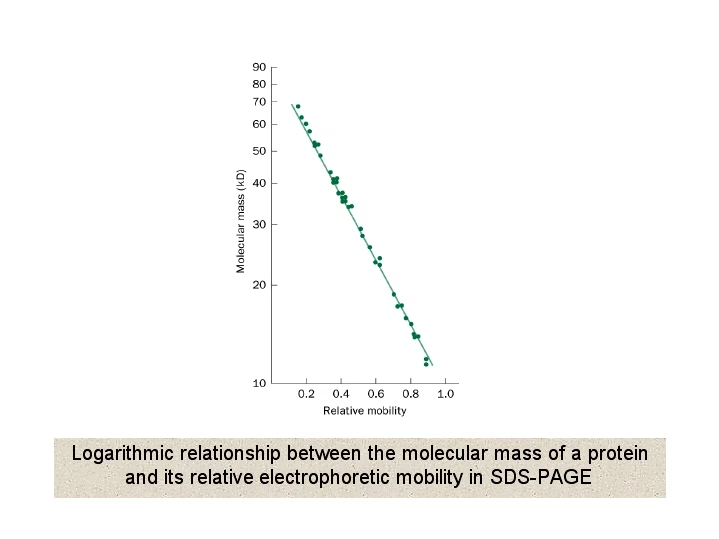
Efter præparationen påføres proteinblandingen på en polyacrylamidgel. Gelen fungerer som et molekylært si, der adskiller proteiner baseret på deres størrelse. Når en elektrisk spændingsforskel påføres, drives SDS-belagte proteiner, som nu er negativt ladede, gennem gelmatrixen mod den positive elektrode. Større protein-SDS-partikler møder mere modstand og bevæger sig langsommere gennem gelens porer, mens mindre partikler nemmere passerer igennem og migrerer hurtigere. Afstanden, et protein/SDS-partikel tilbagelægger fra gelens top, måles og divideres med sporfarvens tilbagelagte afstand for at opnå den relative migration (Rf). Molekylvægten (Mr) bestemmes derefter ved at sammenligne denne værdi med en logaritmisk plot, der er afledt af Rf-værdierne og Mr-værdierne for kendte referenceproteiner (også kaldet molekylvægtsstandarder).
Fra et praktisk synspunkt er acrylamidkoncentrationen i gelen (angivet som %T) afgørende for separationen. Lave procentgeler (f.eks. 4-8% T) har større porer og bruges typisk til at adskille større proteiner, mens høje procentgeler (f.eks. 15-20% T) har mindre porer og er bedre egnet til at adskille mindre proteiner. Koncentrationer uden for området 4-20% T er sjældent anvendt i rutinebrug, da gelerne enten bliver for skrøbelige eller for skøre til fysisk håndtering.
Den Mystiske Migration af Helikale Membranproteiner
Mens de fleste globulære, vandopløselige proteiner opfører sig forudsigeligt på SDS-PAGE, er dette sjældent tilfældet for helikale transmembranproteiner (TM-proteiner). Disse makromolekyler er fundamentale for mange biologiske processer, idet de udgør en betydelig del af det menneskelige genom (20-30%) og flertallet af lægemiddelmål. Deres korrekte identifikation og karakterisering er derfor afgørende for både grundforskning og lægemiddeludvikling.
Problemet opstår, fordi TM-proteiner ofte udviser anomal migration, hvilket betyder, at de migrerer til positioner, der ikke stemmer overens med deres faktiske molekylvægt. Et klassisk eksempel er bovint rhodopsin, et 39 kDa stort G-proteinkoblet receptor, der ofte migrerer som et protein på kun 30 kDa på SDS-PAGE. Denne afvigelse kan skyldes flere faktorer, herunder den høje hydrofobicitet af membranproteiner og deres tendens til at binde SDS i større mængder end vandopløselige polypeptider. En forhøjet SDS-binding kan potentielt ændre protein/SDS-partiklens effektive størrelse og nettoladning på uforudsigelig vis.
I årtier har det været umuligt at forudsige retningen og omfanget af denne anomale migration. Membranproteiner har skiftevis udvist reduceret, ækvivalent eller øget gelmobilitet i forhold til referenceproteiner. Når proteinidentiteten er kendt eller kan bekræftes via andre metoder, kan disse forskelle ofte ignoreres. Men i mange tilfælde, især ved analyse af komplekse vævs- eller celleekstrakter, rejser anomal migration spørgsmål om proteinfoldning, oligomer organisation, proteolytisk spaltning, posttranslationelle modifikationer, alternativ splejsning, antistofkrydsreaktion eller nedbrydning. Dette gør nøjagtige molekylvægtsestimater afgørende for proteinidentifikation.
Nøglen til Forståelse: Akrylamidkoncentrationens Afgørende Rolle
Ny banebrydende forskning har nu kvantificeret den anomale SDS-PAGE-fraktionering af helikale membranproteiner ved at sammenligne den relative mobilitet af de novo designede TM-mimetiske polypeptider med typiske vandopløselige referenceproteiner på Laemmli-geler med varierende akrylamidkoncentration (fra 11-18% T). Resultaterne er bemærkelsesværdige: Det viser sig, at både nettoladningen og den effektive molekylære størrelse blandt de migrerende TM-mimetiske arter overstiger dem for de tilsvarende referenceproteiner. Endnu vigtigere er det, at gelens akrylamidkoncentration dikterer indflydelsen af disse to faktorer på retningen og omfanget af den anomale migration.
Dette fund peger på et komplekst samspil mellem protein/SDS-partiklens nettoladning, dens effektive molekylære størrelse og den tilgængelige plads inden for akrylamidgelmatrixen. På geler med lav akrylamidkoncentration (under et bestemt ækvivalent mobilitetspunkt, Teq) dominerer den øgede nettoladning Rf-værdien, hvilket resulterer i en øget mobilitet. Dette betyder, at membranproteiner kan synes at være mindre, end de er. Men når akrylamidkoncentrationen stiger, bliver migrationen i stigende grad hæmmet af den større partikelstørrelse, hvilket fører til en gradvis reduktion i gelmobiliteten og i sidste ende et 'skifte' til reduceret mobilitet, når Teq overskrides. Dette forklarer, hvorfor større helikale membranproteiner kan udvise øget mobilitet på lavprocentgeler, mens mindre helikale membranproteiner kan udvise reduceret mobilitet på højprocentgeler. Ethvert element, der ændrer molekylstørrelsen, formen og/eller nettoladningen af polypeptid/SDS-partiklen, forventes at påvirke SDS-PAGE-migrationen på en kompleks måde, der afhænger af både akrylamidkoncentration og molekylvægt.
Kvantificering og Forudsigelse af Anomal Migration
For at imødegå udfordringen med anomal migration udviklede forskerne algoritmer baseret på de omfattende data indsamlet fra TM-mimetika og referenceproteiner. Disse algoritmer er designet til at kompensere for den differentielle effekt af akrylamidkoncentration på SDS-PAGE-mobiliteten af en række naturlige membranproteiner. Ved at anvende disse algoritmer kan forskere nu forudsige den anomale migration af membranproteiner i forhold til referencepolypeptider, hvilket i høj grad letter deres identifikation ud fra molekylvægt i SDS-PAGE-applikationer.
De anvendte TM-mimetika blev produceret ud fra peptider og derefter selvpolymeriseret, hvilket skabte en serie af kontrolmolekyler med veldefinerede egenskaber. Ved at analysere disse på forskellige geler og plotte deres relative mobilitet (log Rf) som funktion af akrylamidkoncentrationen (T) – en metode kendt som Ferguson-plots – kunne forskerne systematisk kvantificere effekten af gelmatrixen på migrationen. Denne detaljerede analyse afslørede de underliggende principper, der styrer den anomale migration, og gjorde det muligt at udvikle de korrigerende algoritmer.
Praktiske Anvendelser og Fremtidsperspektiver
Resultaterne af denne forskning har vidtrækkende konsekvenser for alle, der arbejder med proteinanalyse. For det første giver det en unik og ligetil metode til at forudsige anomal migration af membranproteiner. Dette betyder, at selv når proteinidentiteten er ukendt i komplekse prøver, kan en mere præcis molekylvægt bestemmes, hvilket er afgørende for identifikation.
For det andet åbner det muligheden for at optimere SDS-PAGE-betingelserne. Hvis man kan forstå, hvordan akrylamidkoncentrationen påvirker migrationen, kan man vælge den optimale gelkoncentration for at minimere anomalier eller endda bruge flere gelkoncentrationer til at bekræfte proteinets sande størrelse. Forestil dig at kunne identificere helikale membranproteiner med vandopløselige referenceproteiner ved at vælge geler så tæt på Teq som muligt. Dette ville forenkle mange eksperimentelle opsætninger og øge pålideligheden af resultaterne.
Det er dog vigtigt at bemærke, at nøjagtigheden af de nye algoritmer er mest præcis, når de anvendes på Laemmli-geler med den samme bis-acrylamidkoncentration, som blev brugt i studiet, da faktorer som elektroforesebuffersystemet og tværbinderkoncentrationen også kan påvirke migrationen. Ikke desto mindre er dette et massivt skridt fremad. På længere sigt kan TM-mimetika potentielt bruges som nye størrelsesstandarder, der er specifikt designet til at matche membranproteinernes adfærd på SDS-PAGE. I applikationer, hvor proteinet/proteinerne er ukendte, kan sådanne reagenser vise sig at være uundværlige.
Denne forskning understreger vigtigheden af at forstå de finere detaljer i almindelige laboratorieteknikker. Ved at afkode mysteriet bag membranproteiners anomale migration har forskere ikke blot løst et årti gammelt problem, men også forbedret vores evne til at analysere og identificere en af de vigtigste klasser af biomolekyler, hvilket vil have en dybtgående indvirkning på fremtidig biokemisk forskning og lægemiddeludvikling.
Sammenligning af Proteinmigration på SDS-PAGE
| Egenskab / Proteintype | Vandopløselige Proteiner | Helikale Membranproteiner |
|---|---|---|
| SDS-binding | Standardiseret, forudsigelig | Forhøjet, variabel |
| Effektiv Størrelse (på gel) | Tæt på faktisk molekylvægt | Ofte afvigende (større eller mindre) |
| Netto Ladning (efter SDS) | Ensartet negativ | Forhøjet negativ (pga. mere SDS) |
| Forudsigelighed på SDS-PAGE | Høj, molekylvægt let bestemmelig | Lav, anomal migration hyppig |
| Indflydelse af Akrylamidkoncentration | Primært for separationsområde | Afgørende for retning og omfang af anomalier |
| Identifikation | Relativt ligetil | Udfordrende uden specialviden/algoritmer |
Ofte Stillede Spørgsmål (FAQ)
Hvad er anomal migration på SDS-PAGE?
Anomal migration refererer til fænomenet, hvor et protein migrerer på en SDS-PAGE-gel til en position, der ikke stemmer overens med dets sande molekylvægt. For helikale membranproteiner betyder det ofte, at de ser ud til at være enten større eller mindre, end de faktisk er.
Hvorfor er det vigtigt at forstå membranproteiners migration?
Membranproteiner er afgørende for mange biologiske funktioner og udgør en stor del af de lægemiddelmål, der studeres i farmaceutisk forskning. Nøjagtig bestemmelse af deres molekylvægt er afgørende for deres identifikation, karakterisering og forståelse af deres funktion, foldning og eventuelle modifikationer.
Hvordan kan akrylamidkoncentration påvirke resultaterne?
Forskningen viser, at akrylamidkoncentrationen i gelen er en nøglefaktor for retningen og omfanget af anomal migration for membranproteiner. På geler med lav koncentration kan membranproteiner synes at være mindre (migrere hurtigere), mens de på geler med høj koncentration kan synes at være større (migrere langsommere) end deres faktiske størrelse. Ved at forstå denne sammenhæng kan man justere gelkoncentrationen for at opnå mere præcise resultater.
Kan denne forskning hjælpe med at identificere ukendte proteiner?
Ja, absolut. Ved at anvende de nye algoritmer, der er afledt af denne forskning, kan forskere nu kompensere for den anomale migration. Dette betyder, at selv for ukendte helikale membranproteiner i komplekse prøver, kan en mere præcis molekylvægt estimeres, hvilket er afgørende for at indsnævre mulighederne og ultimativt identificere proteinet.
Er der begrænsninger ved de nye algoritmer?
Algoritmerne er mest nøjagtige, når de anvendes på Laemmli-geler med specifikke buffer- og tværbinderkoncentrationer, som anvendt i studiet. Andre elektroforesebuffersystemer eller variationer i tværbinderkoncentrationen kan påvirke mobiliteten og dermed nøjagtigheden af forudsigelserne. Ikke desto mindre repræsenterer de et betydeligt fremskridt.
Hvis du vil læse andre artikler, der ligner Ny Indsigt i Proteinseparation: Membranproteiners Mystiske Migration, kan du besøge kategorien Mobil.