11/10/2025
I en verden, hvor behovet for at forstå og analysere komplekse biologiske og kemiske prøver konstant vokser, står forskere og ingeniører over for store udfordringer. Traditionelle metoder, selvom de er kraftfulde, har ofte begrænsninger, når det kommer til at håndtere den enorme kompleksitet og det brede dynamiske område, der findes i virkelige prøver. Det er her, High Field Asymmetric Waveform Ion Mobility Spectrometry, bedre kendt som FAIMS, træder ind som en banebrydende teknologi. FAIMS er en atmosfærisk tryk ionmobilitetsteknik, der adskiller gasfaseioner baseret på deres adfærd i stærke og svage elektriske felter. Denne unikke tilgang gør det muligt at opnå en hidtil uset separation og renhed af ioner, hvilket er afgørende for præcise analyser.
FAIMS er let at integrere med elektrosprayionisering (ESI) og er blevet implementeret som en ekstra adskillelsestilstand mellem væskekromatografi (LC) og massespektrometri (MS) i proteomiske studier. Dens styrke ligger i, at FAIMS-adskillelse er ortogonal til både LC og MS. Dette betyder, at den tilføjer en helt ny dimension af adskillelse, der ikke er afhængig af de samme egenskaber (f.eks. hydrofobicitet i LC eller masse-til-ladning i MS). Resultatet er en forbedret on-line fraktionering, som markant forbedrer detektionen af peptider i komplekse prøver. Ved at filtrere kemisk støj og fjerne interfererende ionarter forbedrer FAIMS det dynamiske område og dermed detektionsgrænserne for ioner. Det kan også bruges til at vælge peptidladningstilstande, der er optimale for identifikation ved tandem MS. Lad os dykke dybere ned i, hvorfor denne teknologi er så kritisk, og hvordan den fungerer.
- Hvorfor er Selektivitet af Gasfaseioner Afgørende?
- FAIMS: Grundlæggende Koncepter og Terminologi
- Udviklingen af ESI-FAIMS-MS
- Sammenligning af FAIMS-enhedstyper
- Fordele ved FAIMS i Avanceret Analyse
- Udfordringer og Fremtidsperspektiver
- Ofte Stillede Spørgsmål om FAIMS
- Hvad er den primære funktion af FAIMS?
- Hvordan adskiller FAIMS sig fra traditionel massespektrometri (MS) eller væskekromatografi (LC)?
- Hvad betyder 'transparent tilstand' i FAIMS?
- Hvad er fordelene ved at bruge helium (He) som bærergas i FAIMS?
- Hvad er trade-off'en mellem følsomhed og selektivitet i FAIMS?
Hvorfor er Selektivitet af Gasfaseioner Afgørende?
Identifikation af proteiner fra peptidfraktionering ved væskekromatografi koblet til et massespektrometer (LC-MS) er en standardprocedure inden for nuværende biologisk forskning. I den typiske 'shotgun' eller 'bottom-up' tilgang bliver proteiner enzymatisk fordøjet til peptider, som derefter adskilles af højtydende væskekromatografi (HPLC). Kromatografikolonnen kobles til et massespektrometer via elektrosprayionisering (ESI). Udfordringen opstår, når man skal identificere og kvantificere tusindvis af proteiner i komplekse prøver, såsom cellelysat. Massespektrometerets evne til at vælge en peptidprecursorion til fragmentering og efterfølgende identifikation er begrænset af dets arbejdscyklus (hvor mange massespektre der kan opnås pr. tidsenhed), opløsningsevne (evnen til at skelne mellem precursorioner med lignende masse) og dynamiske område (den største og mindste mængde analyt, der giver en lineær respons fra detektoren).
I data-afhængig erhvervelse (DDA) vælges den mest rigelige ion for fragmentering, og så videre. Hvis massespektrometerets arbejdscyklus er utilstrækkelig til at prøve alle precursorioner i en scanning, vil de mindst rigelige ioner ikke blive valgt. Selv med høj massepræcision øger større prøvekompleksitet sandsynligheden for, at flere precursorer fragmenteres samtidigt (hvilket resulterer i vanskeligt fortolkbare kimære spektre), eller at en mindre rigelig precursor maskeres af en mere rigelig. For at en precursorion kan vælges til fragmentering, skal den også kunne skelnes fra baggrundsstøj. Selvom massespektrometre fortsat forbedres, er effektiv prøvetagning af hver komponent i et komplekst proteindigest stadig uden for rækkevidde af et enkelt LC-MS-eksperiment. Dette problem håndteres typisk ved en form for fraktionering forud for LC-MS-analyse, men dette øger prøvebehovet, bidrager til prøvetab og øger variabiliteten. Gasfasefraktionering, som FAIMS tilbyder, undgår manuel prøvehåndtering og forbedrer dynamisk område ved at filtrere kemisk støjreduktion.
FAIMS: Grundlæggende Koncepter og Terminologi
FAIMS er også kendt som differentiel mobilitetsspektrometri (DMS). Begrebet beskriver, hvordan gasfaseioner adskilles baseret på deres karakteristiske forskelle i mobilitet i høje og lave elektriske felter. Ioner, der accelereres gennem et gasmedium af et elektrisk felt (E), når hurtigt en stabil hastighed, hvis størrelse er direkte proportional med ionens ladning og omvendt proportional med ionens kollisionstværsnit (dvs. størrelse). Hastigheden i forhold til den elektriske feltstyrke rapporteres som dens mobilitet K. Ved lave feltstyrker forbliver K konstant, men når E øges, forårsager opvarmning, at K vs. E bliver ikke-lineær. Disse ikke-lineære reaktioner generaliseres som tre typer: Type A ioner øger mobiliteten ved højt felt (f.eks. små molekyler, der afklynger sig fra addukter); Type C ioner falder i mobilitet (f.eks. peptider, der folder sig ud); og Type B ioner øger mobiliteten i starten, men falder i mobilitet, når E øges på grund af højenergi kollisioner.
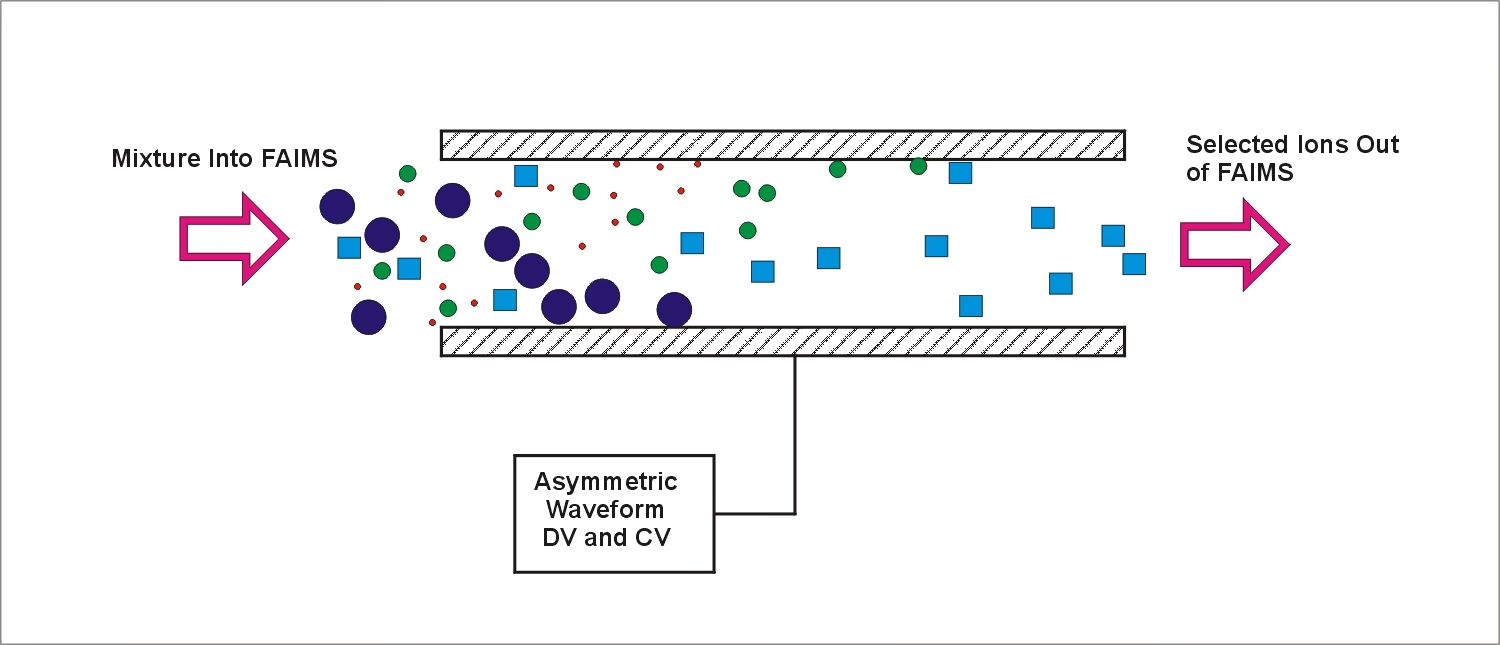
I FAIMS bæres gasfaseioner af en strøm af bærergas mellem to elektroder i en retning vinkelret på E. E genereres som en asymmetrisk bølgeform, der veksler mellem en høj feltspænding af én polaritet og en lav feltspænding af den modsatte polaritet. Størrelsen af bølgeformens højfeltsdel rapporteres som dispersionsspændingen (DV). Varigheden af bølgeformens lavfeltsdel er længere end højfeltsdelen. En ion i feltet vil skifte mellem at bevæge sig mod den ene eller den anden elektrode, når feltet svinger i polaritet. Hvis der ikke er nogen forskel i ionens mobilitet i det høje og lave felt, vil der ikke være nogen nettoforskydning mod nogen af elektroderne, og den vil forlade FAIMS-enheden og kan detekteres. Hvis en ion har en højere mobilitet i det høje eller lave felt, vil den opleve en nettoforskydning mod en elektrode. En lille jævnstrømskompensationsspænding (CV) tilføjet bølgeformen vil forskyde nettoforskydningen og ændre, hvilken delmængde af ioner der passerer gennem FAIMS-enheden til detektoren. I modsætning til traditionel drift tube ionmobilitetsspektrometri (IMS), hvor analytionstrømmen samples i diskrete pakker, er FAIMS en kontinuerlig filtreringsteknik, der tillader uafbrudt prøvetagning af ionstrømmen, men kun for den delmængde af ionpopulationen, der tillades af den valgte CV.
Udviklingen af ESI-FAIMS-MS
FAIMS blev udviklet i det tidligere Sovjetunionen i begyndelsen af 1980'erne og blev delt med det internationale videnskabelige samfund i begyndelsen af 1990'erne. Både planare (p-FAIMS) og cylindriske (c-FAIMS) elektroder blev beskrevet, og FAIMS-enheder blev koblet til både elektrometerdetektorer og MS. Meget af den tidlige udvikling af FAIMS-MS blev udført af forskere, der anvendte FAIMS-enheder med cylindriske geometrier.
En teknisk udfordring med at koble ESI til FAIMS er at lade analytioner komme ind i FAIMS-enheden, mens et kontrolleret gasmiljø opretholdes indeni. Løsningen var at pumpe et overskud af bærergas ind i FAIMS-enheden, hvilket opretholdt et positivt gastryk i enheden og skabte en strøm af "gardin gas" fra indgangsåbningen. Denne gardin gas hjalp med desolvatisering og blæste neutrale molekyler væk, mens ladede ioner blev trukket ind i enheden af en spændingsbias. Denne tilgang til at koble ESI til FAIMS er universel blandt FAIMS-enheder af alle geometrier.
Cylindrisk FAIMS (c-FAIMS)
Det blev observeret, at følsomheden af en c-FAIMS-enhed (procentdelen af analytioner, der passerede gennem enheden) øges, når DV øges. Med planare FAIMS-elektroder forårsager stigende feltstyrke, at ioner bevæger sig længere under hver cyklus af bølgeformen og kolliderer med elektroderne, hvilket reducerer signalet. I modsætning hertil fokuserer det inhomogene felt, der skabes af de cylindriske elektroder, aktivt ioner ind i en smal region mellem elektroderne. Denne ionfokusering af c-FAIMS begrænser, hvilke typer ioner der kan passere gennem enheden, men det er faktisk til gavn for analyse af peptider. Peptider af interesse i proteomstudier er typisk ≥7 rester lange og udviser type C-adfærd, så en cylindrisk FAIMS, der er tunet til at transmittere peptider, vil i vid udstrækning udelukke korte peptider og små molekyler, der ville bidrage til kemisk støj. C-FAIMS er dog kendt for at have en dårligere arbejdscyklus, da ioner bevæger sig længere, hvilket resulterer i længere residenstider.
Planar FAIMS (p-FAIMS)
De fleste af de seneste fremskridt inden for FAIMS-MS-teknologi har fokuseret på planare FAIMS (p-FAIMS) enheder, der anvender to flade parallelle elektroder snarere end koncentriske cylindre. Der er en række fordele ved p-FAIMS-konfigurationer i forhold til c-FAIMS: den enkle elektrogeometri er mere egnet til miniaturisering, hvilket giver kortere residenstider og hurtigere CV-scanningshastigheder; p-FAIMS-enheder kan betjenes i 'transparent tilstand' ved at sætte elektrodepotentialet til jord, hvilket giver brugeren mulighed for at skifte mellem FAIMS- og ikke-FAIMS-analyser uden at ændre hardware; og p-FAIMS kan opnå højere opløsningsevne. Opløsningsevnen af p-FAIMS er større end c-FAIMS, fordi de parallelle planare elektroder producerer et ensartet elektrisk felt uden fokuseringseffekt. Øget opløsningsevne i p-FAIMS er dog ikke uden omkostninger: uden fokusering til at modvirke diffusion falder iontransmissionen i p-FAIMS eksponentielt med residenstiden, hvilket nødvendiggør en afvejning mellem selektivitet og følsomhed.
Ultra FAIMS (u-FAIMS)
Mikrofabrikerede p-FAIMS-enheder, kaldet ultra FAIMS (u-FAIMS), er blevet udviklet for at opnå ekstremt hurtig CV-scanning. Disse enheder er konstrueret med sammenflettede plader, der skaber flere parallelle mellemrum, typisk kun 35 μm i bredden og 300 μm i længden. Sammenlignet med konventionelle p-FAIMS-enheder, der typisk opnår feltstyrker på ~20 kV/cm, muliggør de små dimensioner af u-FAIMS-enheden feltstyrker op til 60 kV/cm med en DV på kun 214 V. U-FAIMS-enheder kan anvende meget højere feltstyrker end makro-FAIMS-enheder og opnå disse forhøjede feltstyrker med betydeligt mindre strøm. Selvom forhøjede feltstyrker reducerer transmissionseffektiviteten på grund af øget diffusion, kan disse tab delvist opvejes ved at reducere residenstiden. Som med makro-p-FAIMS-enheder fører reduceret residenstid til reduceret opløsningsevne, men i u-FAIMS opvejes dette tab delvist af en øget FAIMS-peakkapacitet, der er et resultat af den forhøjede feltstyrke. U-FAIMS er ideel til applikationer, der kræver en hurtig arbejdscyklus, som f.eks. kvantitative analyser.
Sammenligning af FAIMS-enhedstyper
Valget af FAIMS-design er applikationsspecifikt og kræver en balance mellem opløsningsevne, følsomhed og arbejdscyklus.
| Egenskab | Cylindrisk FAIMS (c-FAIMS) | Planar FAIMS (p-FAIMS) | Ultra FAIMS (u-FAIMS) |
|---|---|---|---|
| Elektrodegeometri | Koncentriske cylindre | Flade, parallelle plader | Mikrofabrikeret, parallelle plader |
| Ionfokusering | Ja (artafhængig) | Nej | Nej |
| Følsomhed | Høj (bedst for peptider) | Variabel (afhænger af residenstid) | Lavere end makro-enheder |
| Opløsningsevne | Lavere | Højere (bedst) | Lavere |
| Arbejdscyklus | Dårlig (lang residenstid) | Hurtigere | Meget hurtig (mikrosekunder) |
| Gennemsigtig Tilstand | Nej (hardware skal fjernes) | Ja | Ja |
| Anvendelse | Generel peptidanalyse | Isomerseparation, høj opløsning | Kvantitative analyser, hurtig filtrering |
Fordele ved FAIMS i Avanceret Analyse
FAIMS er yderst velegnet til implementering som en ekstra adskillelsestilstand mellem LC og MS og hjælper med at adressere nogle af de instrumentelle begrænsninger ved LC-MS-proteomik. On-line prøvefraktionering med FAIMS er robust og yderst reproducerbar, hvilket forbedrer peptididentifikation ved at mindske prøvekompleksiteten. FAIMS muliggør detektion af co-eluerende arter med lignende masse-til-ladning ved at tilvejebringe en adskillelsesdimension, der er ortogonal til både væskekromatografi og massespektrometri. Derudover forbedrer FAIMS det dynamiske område og detektionsgrænserne ved at reducere kemisk støj fra enkeltladede peptider, solvatiserede arter og kemisk baggrund. For eksempel har brugen af FAIMS vist sig at øge antallet af identificerede peptider markant i komplekse prøver, samt at forbedre detektionen af fosfopeptider med op til 60% i visse studier. Den forbedrede selektivitet og følsomhed, som FAIMS giver, er også blevet demonstreret for kvantitativ proteomik, hvor det har ført til forbedret præcision i kvantificering, især ved lave koncentrationer, og forbedret eksperimentel reproducerbarhed.
Udfordringer og Fremtidsperspektiver
Selvom FAIMS er en kraftfuld og robust teknik, der betydeligt kan forbedre LC-MS for proteomforskning, er den endnu ikke bredt vedtaget af proteomlaboratorier. Nogle af hindringerne for forbedret FAIMS-ydelse er grundlæggende, men mange er ingeniørmæssige udfordringer. For eksempel er der i øjeblikket ingen værktøj til at forudsige optimale CV-værdier baseret på peptidsekvens, så CV skal vælges empirisk. Da et peptids adfærd i FAIMS er baseret på intrinsiske egenskaber, burde det i princippet være muligt at forudsige optimale CV'er. Numeriske værdier for den optimale CV for et givet peptid afhænger af flere instrumentelle parametre, herunder design, elektrodimensioner, DV, bølgeformens form og frekvens, elektrodetemperatur, bærergassammensætning og bærergasstrømningshastighed. Yderligere eksperimenter er nødvendige for at opnå en mere fuldstændig forståelse af de underliggende processer, der er involveret i peptidseparation ved hjælp af FAIMS.
Fremtidig udvikling af p-FAIMS-enheder bør fokusere på at eliminere unødvendigt signaltab. Det er sandsynligt, at p-FAIMS vil forblive den foretrukne konfiguration for højopløsningsapplikationer, såsom studier af peptidisomerer og konformere. Mikrofabrikerede u-FAIMS-enheder vil sandsynligvis ikke erstatte makro-p-FAIMS-enheder i alle applikationer, men deres ekstremt hurtige arbejdscyklusser gør dem meget attraktive for kvantitative applikationer, såsom reaktionsmonitoreringseksperimenter, der kræver flere datapunkter for at rekonstruere den kromatografiske peak. Efterhånden som teknikken får større synlighed og gøres kommercielt tilgængelig af flere leverandører, er det sandsynligt, at FAIMS vil opnå større accept inden for proteomikfeltet og blive en del af standardværktøjssættet.
Ofte Stillede Spørgsmål om FAIMS
Her er svar på nogle af de mest almindelige spørgsmål vedrørende FAIMS-teknologien:
Hvad er den primære funktion af FAIMS?
Den primære funktion af FAIMS er at adskille gasfaseioner baseret på deres mobilitetsforskelle i stærke og svage elektriske felter. Dette muliggør on-line fraktionering af komplekse prøver, forbedrer detektionsgrænser og reducerer kemisk støj i massespektrometrianalyser.
Hvordan adskiller FAIMS sig fra traditionel massespektrometri (MS) eller væskekromatografi (LC)?
FAIMS tilføjer en ortogonal adskillelsesdimension til LC og MS. Hvor LC adskiller baseret på interaktioner i en væskefase og MS baseret på masse-til-ladning i vakuum, adskiller FAIMS ioner i gasfasen baseret på deres mobilitetsændringer i varierende elektriske felter ved atmosfærisk tryk. Dette betyder, at den kan løse problemer med co-elution eller lignende masse-til-ladningsforhold, som LC og MS alene ikke kan håndtere.
Hvad betyder 'transparent tilstand' i FAIMS?
'Transparent tilstand' refererer til en driftsmodus, hvor FAIMS-enheden kan deaktiveres (typisk ved at sætte elektrodespændingen til jord), så alle ioner kan passere uhindret til massespektrometeret. Dette gør det muligt at skifte mellem FAIMS-assisterede og ikke-FAIMS-assisterede analyser uden at skulle fjerne hardware. Denne funktion er primært tilgængelig i planare FAIMS-enheder.
Hvad er fordelene ved at bruge helium (He) som bærergas i FAIMS?
Tilsætning af helium til bærergassen (typisk nitrogen) har vist sig at øge transmissionseffektiviteten af peptider markant samt forbedre både opløsningsevne og følsomhed i FAIMS. Helium ændrer ionernes adfærd ved høje feltstyrker, hvilket forstærker felt-afhængigheden af peptider og dermed forbedrer adskillelsen. Dog kan omkostningerne ved helium og dets status som en ikke-vedvarende ressource være en ulempe.
Hvad er trade-off'en mellem følsomhed og selektivitet i FAIMS?
I FAIMS er der ofte en omvendt sammenhæng mellem følsomhed (hvor mange ioner der når detektoren) og selektivitet (hvor præcist ioner kan adskilles). Især i planare FAIMS-enheder, hvor der ikke er nogen fokuseringseffekt, falder iontransmissionen eksponentielt med stigende residenstid, hvilket er nødvendigt for højere opløsningsevne. Det betyder, at for at opnå en meget præcis adskillelse (høj selektivitet) kan man miste en del af signalet (lavere følsomhed), og omvendt. Valget afhænger af den specifikke analyseopgave.
Hvis du vil læse andre artikler, der ligner FAIMS: Fremtidens Højpræcisions Adskillelsesteknologi, kan du besøge kategorien Teknologi.
