08/05/2023
I en verden hvor smartphones er blevet en integreret del af vores dagligdag, har mobile sundhedsapps (mHealth) vundet enorm popularitet. Fra at spore træningsrutiner til at overvåge kroniske sygdomme, tilbyder disse apps bekvemmelighed og potentiale for forbedret sundhedspleje. Men hvem holder øje med dem? Gælder de samme regler for disse digitale værktøjer som for traditionelle medicinske apparater? Dette er et centralt spørgsmål i takt med mHealth-markedets eksplosive vækst. Artiklen her dykker ned i FDA's (Food and Drug Administration) politikker og overvejelser vedrørende regulering af mobile sundhedsapps.
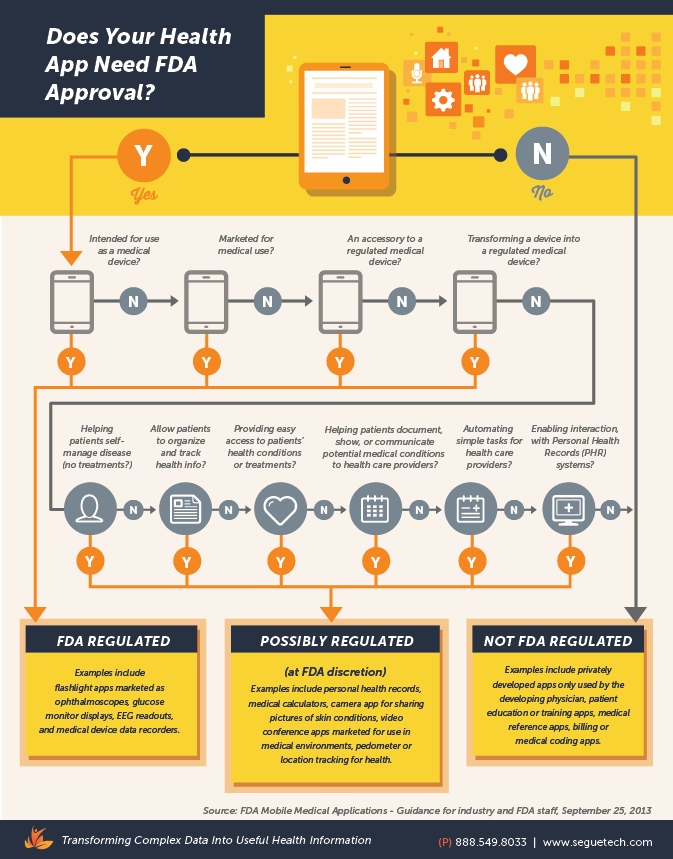
Hvad er Mobile Sundhed (mHealth)?
Mobile sundhed, eller mHealth, dækker over et bredt spektrum af applikationer og teknologier, der anvendes til at forbedre sundhed og velvære. Dette kan omfatte alt fra simple fitness-trackere og kostdagbogsapps til mere avancerede programmer, der kan måle vitale tegn, administrere medicin eller hjælpe med diagnostik. Disse apps kan køre på smartphones, tablets og andre mobile enheder, og de er designet til at give brugere, sundhedspersonale og forskere adgang til sundhedsrelateret information og tjenester. mHealth repræsenterer en betydelig transformation i sundhedssektoren, der muliggør personlig medicin og fjernovervågning.
Gælder FDA's Politikker for Mobile Sundhedsapps?
Ja, FDA's politikker kan anvendes på mobile sundhedsapps, især når disse apps betragtes som medicinsk udstyr. FDA definerer et medicinsk udstyr som ethvert instrument, apparat, implement, maskine, enhed, implatat, in vitro-reagens eller andet lignende eller relateret artikel, som er beregnet til brug i diagnosticering af sygdom eller andre tilstande, eller i helbredelse, lindring, behandling eller forebyggelse af sygdom hos mennesket. Hvis en mobilapp opfylder denne definition, falder den potentielt under FDA's tilsyn. Dette omfatter apps, der bruges til at diagnosticere, behandle, lindre eller forebygge en bestemt sygdom eller tilstand.
Bør FDA Regulere mHealth Enheder?
Spørgsmålet om, hvorvidt FDA bør regulere mHealth-enheder, er komplekst. En af de mest fremtrædende holdninger er, at FDA's eksisterende ramme for regulering af medicinsk udstyr er velegnet til at vurdere og godkende mHealth-enheder. Dette skyldes, at FDA har etableret processer og ekspertise til at sikre sikkerhed og effektivitet af medicinsk udstyr. Det er dog afgørende, at FDA udviser forsigtighed og undgår overregulering. Overregulering kan potentielt hæmme innovation og forsinke adgangen til vigtige sundhedsteknologier for forbrugerne. Det er vigtigt at skelne mellem selve sundhedssoftwaren eller applikationen og den underliggende mobile teknologi. FDA's fokus bør primært være på den funktion, der har medicinsk relevans.

FDA's Tilgang til Regulering
FDA opererer med en risikobaseret tilgang til regulering af medicinsk udstyr. Dette betyder, at enheder klassificeres baseret på deres potentielle risiko for patienterne. Klassifikationerne spænder fra Klasse I (lav risiko) til Klasse III (høj risiko). De fleste mHealth-apps, der falder ind under FDA's jurisdiktion, vil sandsynligvis blive klassificeret som Klasse II (moderat risiko) eller endda Klasse I. Denne klassificering bestemmer, hvilke krav en producent skal opfylde for at få deres produkt på markedet, herunder præ-marked godkendelse eller notifikation. Det er essentielt at forstå, at ikke alle sundheds-apps kræver FDA-godkendelse. Apps, der primært tilbyder generel wellness-information eller fitness-tracking uden påståede medicinske fordele, falder typisk uden for FDA's reguleringsområde.
Udfordringer og Overvejelser
Der er flere udfordringer forbundet med FDA's regulering af mHealth:
- Innovationstempo: Den teknologiske udvikling inden for mHealth sker i et rasende tempo. FDA's reguleringsprocesser kan være langsomme og risikerer at sakke bagud i forhold til nye innovationer.
- Softwareændringer: mHealth-apps opdateres ofte. FDA skal finde en måde at håndtere disse løbende ændringer på uden at bremse udviklingen.
- Dataindsamling og Privatliv: mHealth-apps indsamler ofte følsomme personlige sundhedsoplysninger. FDA's rolle i at sikre databeskyttelse og privatliv er også en vigtig overvejelse, selvom dette ofte falder ind under andre reguleringsorganers ansvarsområder som f.eks. HIPAA i USA.
- International Regulering: mHealth-markedet er globalt. Forskellige lande har forskellige reguleringsrammer, hvilket kan skabe udfordringer for producenter, der opererer internationalt.
Tabel: Sammenligning af Regulering af mHealth vs. Traditionelle Medicinske Enheder
Her er en simpel tabel, der illustrerer nogle forskelle og ligheder i FDA's tilgang:
| Aspekt | mHealth Apps (Medicinsk Formål) | Traditionelle Medicinske Enheder |
|---|---|---|
| Definition | Software der opfylder definitionen af et medicinsk udstyr. | Fysiske apparater, instrumenter, etc., der opfylder definitionen af et medicinsk udstyr. |
| Reguleringsramme | FDA's eksisterende ramme for medicinsk udstyr, tilpasset software. | FDA's etablerede ramme for medicinsk udstyr. |
| Risikoklassificering | Klasse I, II, III baseret på medicinsk risiko. | Klasse I, II, III baseret på medicinsk risiko. |
| Præ-marked Godkendelse | Kræves for visse apps (afhængig af klassificering). | Kræves for visse enheder (afhængig af klassificering). |
| Fokus på Innovation | Udfordring pga. hurtigt skiftende teknologi og softwareopdateringer. | Kan også være en udfordring, men ofte med mere stabile produktcyklusser. |
| Eksempler | Apps til diabetesstyring, EKG-aflæsning, dosisberegning. | Pacemakers, røntgenapparater, implantater. |
Ofte Stillede Spørgsmål (FAQ)
1. Kræver alle sundheds-apps FDA-godkendelse?
Nej, kun de apps, der er designet til et medicinsk formål og opfylder FDA's definition af et medicinsk udstyr, kræver godkendelse. Generelle wellness- og fitness-apps falder typisk uden for dette. Det er vigtigt at undersøge den specifikke funktion af en app.
2. Hvordan kan jeg vide, om en mHealth-app er godkendt af FDA?
Du kan ofte finde information om FDA-godkendelse på appens hjemmeside, i app-butikkens beskrivelse eller ved at søge i FDA's database over godkendte medicinske enheder.

3. Hvad hvis en mHealth-app giver forkert medicinsk rådgivning?
Hvis en app er reguleret af FDA og giver forkert rådgivning, der fører til skade, kan brugeren rapportere dette til FDA. FDA overvåger også markedet for potentielt farlige eller vildledende produkter.
4. Hvem er ansvarlig for reguleringen af sundhedsdata privatliv i mHealth?
Mens FDA fokuserer på sikkerhed og effektivitet af medicinske enheder, er andre myndigheder, som Health and Human Services (HHS) i USA, ansvarlige for at håndhæve regler for sundhedsdata privatliv, såsom HIPAA.
Konklusion
FDA spiller en afgørende rolle i at sikre, at mobile sundhedsapps, der har medicinske formål, er både sikre og effektive. Mens den eksisterende ramme for regulering af medicinsk udstyr tilbyder en grundlæggende struktur, kræver mHealth-sektorens dynamiske natur en fortsat tilpasning og dialog mellem regulatorer og industrien. Målet er at fremme innovation, samtidig med at patientsikkerheden garanteres. For forbrugere er det vigtigt at være opmærksom på appens påståede funktioner og at søge information om dens regulatoriske status, når det er relevant for sundhedsbeslutninger.
Hvis du vil læse andre artikler, der ligner Regulering af Mobile Sundhedsapps, kan du besøge kategorien Teknologi.

