16/08/2022
Insulin, glukose og frie fedtsyrer (FFS) er hjørnestenene i vores krops energistofskifte. De arbejder i et komplekst samspil for at sikre, at vores celler får den energi, de har brug for, samtidig med at overskydende energi lagres til senere brug. Når dette delikate system kommer ud af balance, kan det føre til alvorlige sundhedsproblemer, herunder type 2-diabetes og metabolisk syndrom. Denne artikel vil dykke ned i, hvordan insulin regulerer FFS, og hvordan forstyrrelser i dette samspil kan have vidtrækkende konsekvenser for hele kroppen.
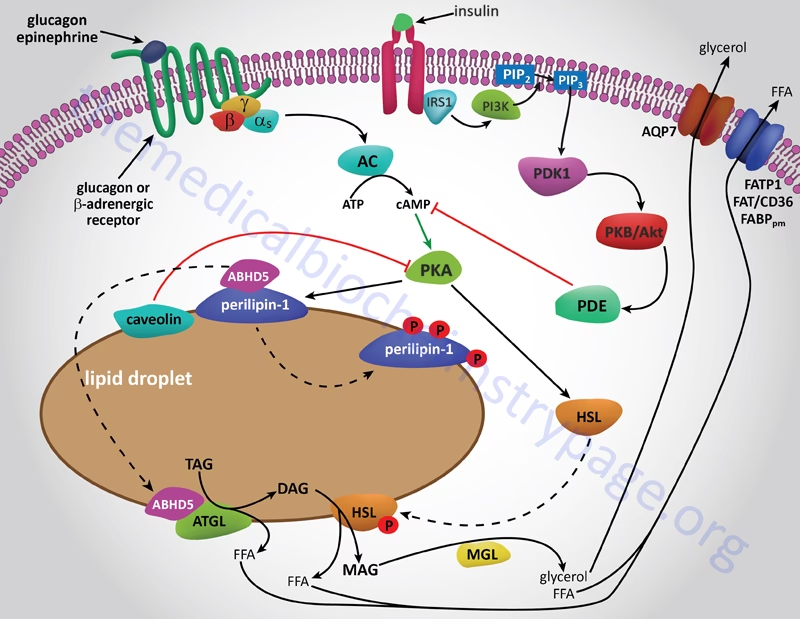
Insulin, et hormon produceret i bugspytkirtlen, er bredt anerkendt for sin rolle i at kontrollere blodsukkeret ved at fremme glukoseoptagelse i muskel- og fedtceller. Men insulins indflydelse strækker sig langt ud over glukose. Det er også en primær regulator af fedt- og proteinmetabolismen. En af insulins vigtigste funktioner i fedtvævet er at undertrykke lipolyse – processen hvor lagret fedt nedbrydes til frie fedtsyrer, der frigives til blodbanen. Når insulin virker effektivt, sikrer det, at fedt lagres sikkert i fedtcellerne. Men i tilfælde af insulinresistens, en tilstand hvor cellerne ikke reagerer optimalt på insulin, bliver denne proces forstyrret, hvilket fører til øgede niveauer af FFS i blodet.
Insulins Rolle i Fedtstofskiftet: En Nøgle til Metabolisk Sundhed
Frie fedtsyrer er essentielle næringsstoffer, der tjener som en vigtig energikilde for kroppen. Historisk set er FFS ofte blevet betragtet som "metaboliske skurke", især når de er forhøjede. Dette skyldes, at kronisk forhøjede FFS-niveauer kan føre til en tilstand kendt som lipotoksicitet, som er forbundet med en række negative metaboliske effekter, herunder forværret glukosetolerance og insulinresistens. Det er endda blevet foreslået, at type 2-diabetes i høj grad er en konsekvens af et forstyrret fedtstofskifte.
Nye forskningsmodeller har imidlertid bidraget til en mere nuanceret forståelse af insulins rolle i FFS-kinetik. En nylig undersøgelse med sunde frivillige under 40 år og med en BMI under 30 kg/m², har foreslået en ny model til at estimere insulins virkning på FFS-lipolyse og -oxidation, hvilket muliggør en måling af fedtvævets insulinfølsomhed (SIFFA). Denne model, der analyserer data fra en insulinmodificeret Hyppigt Samplet Intravenøs Glukosetolerancetest (FSIGT), har afsløret, at FFS-metabolismen er mere følsom over for ændringer i insulin end glukosemetabolismen. Dette antyder et samarbejde snarere end en konkurrence mellem glukose og FFS, hvor FFS potentielt fungerer som en "buffer", der hjælper med at opretholde glukosehomøostase.
Avancerede Modeller og FFS-Kinetik: Nye Indsigter
Tidligere har flere modeller forsøgt at beskrive interaktionen mellem insulin og FFS, men mange var begrænsede af deres kompleksitet, afhængighed af specifikke eksperimentelle protokoller eller ufuldstændig dataudnyttelse. Den nye model adskiller sig ved at give kvantitative mål for FFS's følsomhed over for insulins virkning og oxidation, og den estimerer desuden glukosens bidrag som regulator af FFS-oxidation.
Interessant nok viste studiet, at insulins virkning på FFS (XFFA) indtræffer hurtigere – cirka 4 minutter efter en glukoseudfordring – sammenlignet med insulins virkning på endogen glukose (X), der toppede efter cirka 12 minutter. Dette indikerer, at mekanismen for insulins virkning er forskellig for FFS sammenlignet med glukose. Tidligere antog man, at insulins virkning var identisk for begge, men dette studie tyder på, at insulins effekt på FFS-lipolyse er ekstremt følsom og hurtig.

Modellen for FFS-kinetik, der blev udviklet, bygger på flere forenklende antagelser. For det første påvirker plasma-insulin ikke direkte FFS-kinetik, men virker gennem et "fjernt" rum, hvilket afspejler den tid, det tager for insulin at krydse kapillærerne og udøve sin effekt. For det andet er der defineret nye parametre for insulins virkning på FFS, uafhængigt af insulins virkning på glukose. For det tredje antager modellen, at insulin primært påvirker undertrykkelsen af FFS-lipolyse, mens glukose styrer FFS-oxidation. Dette er i modsætning til tidligere modeller, der ofte antog, at FFS-forsvinden primært skyldtes nedsat lipolyse, mens FFS-oxidation forblev konstant. Den nye models formulering antyder, at FFS-udnyttelse er under direkte og proportional kontrol af glukose, hvilket understøtter et koordineret samspil mellem glukose og FFS, hvor FFS kan fungere som et "bufferbrændstof" for at opretholde glukosehomøostase.
Organ-Specifik Insulinresistens: En Kompleks Symfoni af Ubalance
Insulinresistens er en kompleks tilstand, der kan manifestere sig forskelligt i kroppens organer. Selvom fedme ofte ses som årsagen, tyder forskning på, at inflammation, ofte induceret af kosten, er en central drivkraft.
Hypothalamus: Kontrolcenteret
Mange aspekter af insulinresistens ser ud til at starte i hypothalamus, hjernens kontrolcenter for energibalance og appetit. Hypothalamus koordinerer energiforbrug med energiindtagelse. Overflødige kalorier eller mættede fedtstoffer (især palmitinsyre) kan forårsage inflammation i hypothalamus. Denne inflammation fører til resistens over for mæthedssignaler fra insulin og leptin, hvilket resulterer i øget sult og kalorieindtag. Omvendt kan omega-3-fedtsyrer, som EPA og DHA, reducere inflammation i hypothalamus og dermed forbedre insulinfølsomheden. Det er bemærkelsesværdigt, at inflammation i hypothalamus kan opstå inden for 24 timer efter start på en fedtholdig kost, før der ses vægtøgning i fedtvævet. Dette understreger hypothalamus' centrale rolle i udviklingen af insulinresistens.
Fedtvæv: Kroppens Fedtdepot
Fedtvæv er kroppens primære sted for sikker lagring af overskydende energi. Så længe fedtcellerne er sunde og reagerer på insulin, er der ingen alvorlige metaboliske konsekvenser, udover overvægt. Dog har fedtceller ikke ubegrænset kapacitet. Overudvidelse af eksisterende fedtceller kan skabe hypoxi (iltmangel), hvilket aktiverer inflammatoriske veje. Denne inflammation skaber insulinresistens i fedtcellen. Normalt er insulin et anti-lipolytisk hormon, der hæmmer hormonfølsom lipase (HSL) og adipose triglycerid lipase (ATGL), som er nødvendige for at frigive lagrede fedtsyrer. Med inflammation og insulinresistens i fedtcellerne frigives højere niveauer af FFS til cirkulationen, som derefter optages af andre organer som leveren og skeletmuskulaturen, der ikke kan lagre store mængder fedt sikkert. Dette fører til lipotoksicitet og yderligere systemisk insulinresistens. Desuden tiltrækkes pro-inflammatoriske M1-makrofager til fedtvævet, hvilket yderligere forværrer insulinresistensen og lipolysen. Denne proces skaber en ond cirkel, hvor insulinresistens fører til øget sult og øget strøm af FFS både ind og ud af fedtvævet.
Leveren: Det Centrale "Produktionsanlæg"
Leveren behandler og lagrer næringsstoffer, men i modsætning til fedtvævet kan den ikke sikkert lagre store mængder fedt. En af de første metaboliske konsekvenser af insulinresistens er ophobning af fedtaflejringer i leveren, kendt som ikke-alkoholisk fedtleversygdom (NAFLD). NAFLD er udbredt, og det forventes, at en stor del af befolkningen vil lide af det i fremtiden. I leveren aktiveres interne makrofager (Kupffer-celler), som frigiver cytokiner, der fremmer inflammation. Ligesom i hypothalamus kan NAFLD udvikles hurtigt – inden for 3 dage efter en fedtholdig kost. Leverens insulinresistens er tæt forbundet med fedtsyreniveauerne i leveren, og ikke nødvendigvis med mængden af visceralt fedt. Ophobning af diacylglycerider (DAG) i leveren er en god klinisk markør for kronisk insulinresistens i dette organ. Insulinresistens i leveren afspejles også i dysfunktion i lipoprotein-syntesen, med øgede VLDL-partikler og nedsatte HDL-niveauer, hvilket kan måles via TG/HDL-forholdet.

Skeletmuskulaturen: Glukoseoptagelsens Hovedsæde
Skeletmuskulaturen er det primære sted for glukoseoptagelse. I modsætning til fedtvævet er der minimal makrofag-infiltration i muskler ved insulinresistens. I stedet menes cytokiner fra andre organer (fedtvæv og lever) at påvirke musklens insulinfølsomhed. Mættede fedtsyrer kan reducere fedtsyreoxidation i musklerne via TLR-4-receptorer, og ceramid-niveauer er stærkt forbundet med insulinresistens i musklerne. En unik egenskab ved skeletmuskulaturen er, at træning kan overvinde insulinresistens i dette organ ved at øge oxidationen af akkumulerede fedtsyrer og forbedre glukosemetabolisme i cellen. Dette understreger, at de molekylære drivere af insulinresistens kan variere fra organ til organ.
Bugspytkirtlen: Insulinproducenten
Bugspytkirtlens beta-celler er ansvarlige for at frigive insulin som reaktion på blodsukkerniveauer. Selvom beta-cellerne normalt ikke betragtes som direkte mål for insulinresistens, er de meget modtagelige for toksicitet medieret af inflammatoriske stoffer. Især 12-HETE, et produkt af arachidonsyre (en omega-6 fedtsyre), er meget giftig for beta-celler. Ødelæggelse af beta-cellerne kan føre til, at bugspytkirtlen ikke længere kan opretholde kompenserende insulinniveauer, hvilket hurtigt fører til udviklingen af type 2-diabetes.
Delvis Hæmning af Fedtvævslipolyse: En Lovende Behandlingsstrategi?
Givet den centrale rolle, som forhøjede frie fedtsyrer spiller i udviklingen af insulinresistens og lipotoksicitet, er der stigende interesse for at undersøge, om delvis hæmning af fedtvævslipolyse kan forbedre glukosemetabolismen og insulinfølsomheden. Forskning tyder på, at en sådan strategi faktisk kan være gavnlig. Studier har vist, at delvis hæmning af lipolyse i fedtvævet, for eksempel gennem modulering af enzymer som ATGL (Adipose Triglyceride Lipase) og HSL (Hormone-Sensitive Lipase), kan føre til forbedret glukosemetabolisme og øget insulinfølsomhed, selv uden betydeligt fedttab. Dette indikerer, at det ikke kun er mængden af fedt, men også dynamikken i fedtomsætningen, der er afgørende for metabolisk sundhed. Ved at kontrollere frigivelsen af FFS fra fedtdepoterne kan man potentielt mindske den metaboliske belastning på andre organer og genoprette insulinfølsomheden.
Ofte Stillede Spørgsmål
| Spørgsmål | Svar |
|---|---|
| Er frie fedtsyrer reguleret af insulin? | Ja, absolut. Insulin regulerer delvist frie fedtsyrer (FFS). Dets primære virkning i fedtvævet er at undertrykke lipolyse (nedbrydning af lagret fedt og frigivelse af FFS) og at fremme optagelsen af glukose til dannelse af fedt. Ny forskning viser, at FFS-metabolismen er mere følsom over for insulin end glukosemetabolismen. |
| Stimulerer insulin fedtsyretransport? | Insulin stimulerer ikke direkte transport af frit cirkulerende fedtsyrer ind i cellerne på samme måde, som det stimulerer glukosetransport (via GLUT-4). Dog aktiverer insulin lipoprotein lipase på fedtcellernes overflade, hvilket fører til frigivelse af fedtsyrer fra lipoproteiner, som derefter kan optages af fedtceller til lagring. Så insulin fremmer fedtlagring og hæmmer frigivelse af lagret fedt. |
| Hvordan påvirker insulin fedtvæv? | Insulin er afgørende for fedtvævets funktion. Det undertrykker lipolyse, hvilket forhindrer overdreven frigivelse af frie fedtsyrer til blodbanen. Desuden fremmer det optagelsen af glukose i fedtcellerne, som derefter kan omdannes til triglycerider og lagres som fedt. Dette sikrer en sund og sikker fedtlagring, så længe fedtcellerne er velfungerende og insulinfølsomme. |
| Kan delvis hæmning af fedtvævslipolyse forbedre glukosemetabolisme og insulinfølsomhed? | Ja, forskning tyder på, at delvis hæmning af fedtvævslipolyse kan forbedre både glukosemetabolisme og insulinfølsomhed. Dette skyldes, at reduceret frigivelse af frie fedtsyrer mindsker lipotoksicitet i andre organer (som lever og muskler), hvilket kan genoprette deres insulinfølsomhed, selv uden et betydeligt vægttab. |
Samlet set er interaktionen mellem insulin, glukose og frie fedtsyrer fundamentalt for vores metaboliske sundhed. Forståelsen af, hvordan inflammation, kost og organ-specifikke processer påvirker denne balance, er afgørende for at udvikle effektive strategier til forebyggelse og behandling af metaboliske sygdomme som type 2-diabetes. Fremtidig forskning vil fortsat afdække de finere nuancer af dette komplekse samspil, hvilket kan bane vejen for mere målrettede behandlinger.
Hvis du vil læse andre artikler, der ligner Insulin, Frie Fedtsyrer og Dit Stofskifte, kan du besøge kategorien Mobil.
