12/01/2024
Et knoglebrud er en almindelig skade, som de fleste af os vil opleve mindst én gang i livet. Selvom det kan virke som en simpel, men smertefuld begivenhed, sætter et knoglebrud en utrolig kompleks og fascinerende helingsproces i gang i kroppen. Fra det øjeblik et knoglebrud opstår, arbejder kroppen intenst på at reparere skaden, genoprette stabiliteten og genopbygge det beskadigede væv. Men hvad er det præcist, der driver denne helingsproces? Nyere forskning peger på en særlig type celler, kendt som Endoteliale Forløberceller (EPC'er), som spiller en afgørende rolle i denne reparation. Disse celler er afgørende for dannelsen af nye blodkar, en proces der er uundværlig for knogleheling.
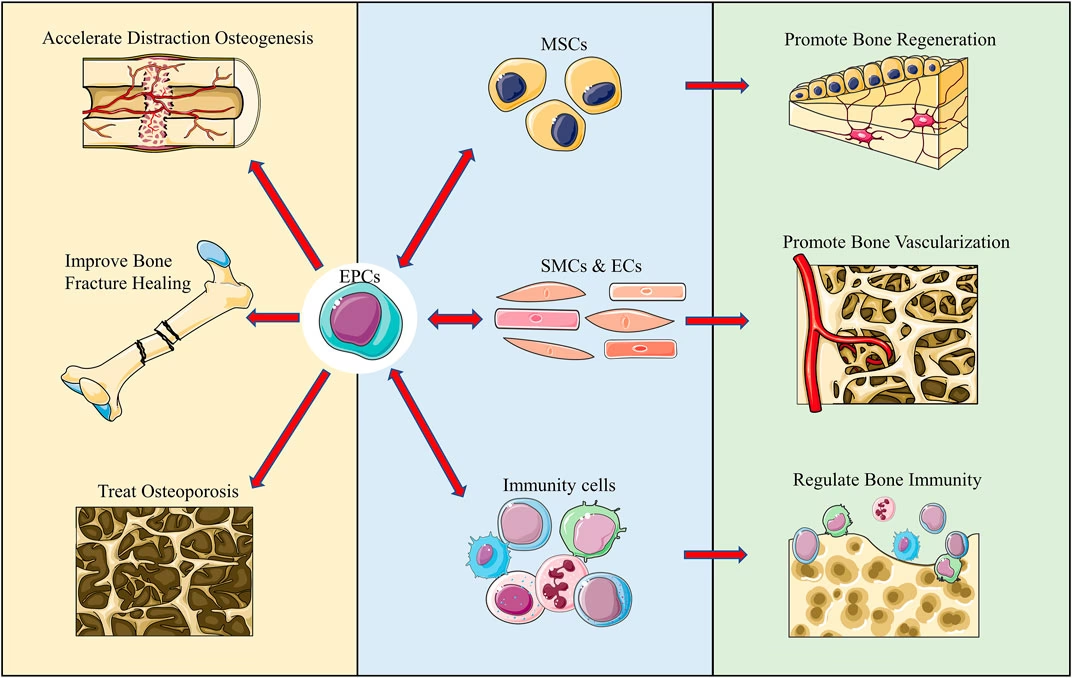
Knogleheling er en biologisk proces, der kræver en rigelig forsyning af ilt og næringsstoffer, som udelukkende leveres via blodbanen. Uden tilstrækkelig blodforsyning ville selv de mest avancerede cellulære mekanismer have svært ved at fungere effektivt. Når et knoglebrud indtræffer, beskadiges ikke kun knoglevævet, men ofte også de omgivende blodkar, hvilket skaber et område med reduceret blodgennemstrømning – et hypoksisk miljø. For at overvinde dette og fremme helingen er kroppen afhængig af en proces kaldet neovaskularisering, som er nydannelsen af blodkar. Denne proces er fundamental for at genoprette et optimalt helingsmiljø.
Vores forståelse af knogleheling har udviklet sig betydeligt gennem årene. Tidligere mente man, at de nye blodkar primært opstod ved knopskydning fra eksisterende kar (angiogenese). Men forskning har nu afsløret, at en anden proces, kaldet vasculogenese, hvor nye blodkar dannes de novo fra forløberceller, også spiller en kritisk rolle. Og det er her, de endoteliale forløberceller kommer ind i billedet. Disse specialiserede celler, der primært stammer fra knoglemarven, er kroppens egne "byggesten" til at konstruere nye blodkar, hvor behovet er størst, herunder ved et knoglebrud.
Hvad er Endoteliale Forløberceller (EPC'er)?
Endoteliale Forløberceller, ofte forkortet EPC'er, er en unik population af stamcellelignende celler, der har den bemærkelsesværdige evne til at differentiere sig til endotelceller – de celler, der beklæder indersiden af vores blodkar. Disse celler er afgørende for vedligeholdelsen af vores vaskulære system, men deres rolle bliver særligt prominent i situationer med vævsskade, såsom et knoglebrud. De fungerer som en slags "reparationshold", der kan mobiliseres fra deres oprindelsessted for at bidrage til genopbygningen af beskadigede blodkar eller skabelsen af helt nye.
Selvom EPC'er findes i perifert blod, er deres primære reservoir knoglemarven. Det er her, de produceres og opbevares, klar til at blive sendt ud, når kroppen signalerer et behov. Deres evne til at migrere til skadede områder og bidrage til vasculogenese (dannelse af nye blodkar fra forløberceller) og angiogenese (dannelse af nye blodkar fra eksisterende blodkar) gør dem til essentielle aktører i mange fysiologiske og patologiske processer, herunder sårheling, iskæmisk sygdom og altså også knoglebrudsheling.
Knoglebrudsprocessen og Vaskulariseringens Tidslinje
Når et knoglebrud opstår, gennemgår helingsprocessen typisk flere overlappende faser: en inflammatorisk fase, en reparativ fase og en remodelleringsfase. I den tidlige reparative fase, omkring dag 7 efter bruddet, ser man en markant stigning i neovaskulariseringsaktiviteten på brudstedet. Dette blev bekræftet gennem serielle undersøgelser med Laser Doppler perfusionsbilleddannelse og histologisk kapillærtæthedsanalyse, som viste, at nydannelsen af blodkar toppede i denne tidlige fase af endokondral ossifikation – processen hvor brusk omdannes til knogle. Denne tidsmæssige sammenhæng understreger, hvor kritisk en tidlig og robust blodforsyning er for at etablere det rette miljø for knogledannelse.
Den hurtige etablering af et nyt vaskulært netværk er ikke blot en forudsætning for at levere ilt og næringsstoffer, men også for at fjerne affaldsstoffer og tiltrække andre celler, der er nødvendige for helingen, såsom osteoblaster (knogledannende celler) og osteoklaster (knoglenedbrydende celler, der remodellerer knoglen). Uden en effektiv neovaskularisering ville helingsprocessen forlænges betydeligt, og risikoen for komplikationer som f.eks. manglende heling (non-union) ville stige dramatisk.
Beviser for Knoglemarvsafledte EPC'ers Pivotal Rolle
For at bekræfte den præcise rolle og oprindelse af EPC'er i knoglebrudsheling, har forskere udført en række stringente eksperimenter. En tidligere rapport havde allerede antydet, at systemisk administration af perifert blod (PB) CD34+ celler, som er en EPC-beriget population, bidrog til knoglebrudsheling via vasculogenese/angiogenese. Men det fysiologiske og patofysiologiske grundlag for EPC'ernes rolle var ikke fuldt ud klarlagt. Derfor undersøgte man hypotesen om, hvorvidt mobilisering og inkorporering af knoglemarvsafledte EPC'er spiller en afgørende rolle for en hensigtsmæssig knoglebrudsheling.
Forskningen anvendte flere metoder til at bevise dette:
- FACS-analyse (Fluorescence-activated cell sorting): Denne teknik viste, at frekvensen af knoglemarvs cKit+Sca1+Lineage- (Lin-) celler og perifere blod Sca1+Lin- celler – som er EPC-berigede fraktioner – steg markant efter et knoglebrud. Dette indikerer, at bruddet udløser en mobilisering af disse celler fra knoglemarven.
- Dobbelt Immunhistokemi: Ved at anvende dobbelt immunhistokemi for CD31 (en markør for endotelceller) og Sca1 (en markør for EPC'er) kunne forskere bekræfte, at Sca1+ EPC-afledt vasculogenese faktisk fandt sted på brudstedet. Dette beviste, at EPC'erne aktivt bidrog til dannelsen af nye blodkar.
- Knoglemarvstransplantation fra Transgene Donorer: Dette var et afgørende eksperiment. Ved at transplantere knoglemarv fra transgene donorer, der udtrykte LacZ (et reportergen) transkriptionelt reguleret af en endotelcelle-specifik Tie-2 promotor, til vildtype-modtagere, fik man direkte bevis. De EPC'er, der bidrog til den forbedrede neovaskularisering på brudstedet, stammede specifikt fra knoglemarven. Dette eliminerer tvivl om cellernes oprindelse.
- Systemisk Administration af GFP+ Celler: Et dyremodelstudie, hvor man systemisk administrerede perifert blod Sca1+Lin- Grønt Fluorescerende Protein (GFP)+ celler, bekræftede yderligere inkorporeringen af de mobiliserede EPC'er i brudstedet, hvor de bidrog til knoglehelingen. GFP gjorde det muligt at spore cellerne og se, hvor de endte.
Disse fund indikerer entydigt, at et knoglebrud kan inducere mobilisering af EPC'er fra knoglemarven til det perifere blod og rekruttering af de mobiliserede EPC'er til brudstederne. Dette forstærker neovaskulariseringen under knoglehelingsprocessen. Samlet set tyder beviserne på, at EPC'er spiller en essentiel rolle i knogleheling ved at fremme et gunstigt miljø gennem netop neovaskularisering i det beskadigede skeletvæv.
Mobilisering og Rekruttering: En Cellenes Rejse
Forestil dig kroppens reaktion på et knoglebrud som en velorkestreret nødsituation. Når bruddet opstår, frigives specifikke signaler – inflammatoriske cytokiner, vækstfaktorer og kemokiner – fra det beskadigede væv. Disse signaler fungerer som en slags "nødråb", der når frem til knoglemarven, hvor EPC'erne befinder sig. Som reaktion på disse signaler begynder EPC'erne at mobilisere sig fra knoglemarven og ud i blodbanen.
Fra blodbanen navigerer disse mobiliserede EPC'er mod brudstedet, tiltrukket af de samme kemiske signaler, der oprindeligt udløste deres frigivelse. Ved ankomsten til det beskadigede område klæber de sig til karvæggen og migrerer ud i vævet. Her begynder de deres vigtige arbejde med at differentiere sig og inkorporere sig i de nydannede blodkarstrukturer. De bliver en integreret del af det nye vaskulære netværk, hvilket genopretter blodforsyningen og sikrer, at ilt, næringsstoffer og andre essentielle komponenter kan nå frem til det helende knoglevæv. Denne præcise og koordinerede rejse fra knoglemarv til brudsted er afgørende for en effektiv og hurtig helingsproces.
Hvorfor er denne Viden Vigtig?
Forståelsen af EPC'ernes afgørende rolle i knoglebrudsheling åbner nye døre for fremtidige terapeutiske strategier. Hvis vi kan manipulere eller forstærke EPC'ernes mobilisering og rekruttering, kan vi potentielt fremskynde helingsprocessen, især hos patienter med nedsat helingskapacitet, såsom ældre, diabetikere eller dem med komplekse brud. Forestil dig muligheden for at give et "boost" til kroppens naturlige helingsmekanismer, hvilket kunne forkorte restitutionstiden og forbedre patienternes livskvalitet markant.
Denne forskning understreger også vigtigheden af at opretholde en sund knoglemarv og et velfungerende vaskulært system for optimal knogleheling. Det giver os indsigt i, hvorfor visse tilstande kan føre til forsinket heling eller non-union, og peger på potentielle mål for intervention. Fremtidig forskning kan fokusere på at identificere de præcise signalveje, der regulerer EPC-mobilisering og -inkorporering, for at udvikle mere målrettede behandlinger.
Sammenligning: Normal Heling vs. Svækket Heling
For at tydeliggøre EPC'ernes betydning, kan vi sammenligne en normal knogleheling med en situation, hvor EPC-aktiviteten er kompromitteret:
| Aspekt | Normal Heling (med optimal EPC-aktivitet) | Svækket Heling (med reduceret EPC-aktivitet) |
|---|---|---|
| Blodforsyning | Hurtig og effektiv nydannelse af et rigt vaskulært netværk, der sikrer optimal ilt- og næringsstoftilførsel til brudstedet. | Langsom eller utilstrækkelig nydannelse af blodkar, hvilket fører til hypoxi (iltmangel) og mangel på essentielle næringsstoffer i helingsområdet. |
| Celleaktivitet | Høj mobilisering af EPC'er fra knoglemarven og effektiv inkorporering i de nydannede kar, hvilket understøtter aktiviteten af osteoblaster og andre helingsceller. | Reduceret mobilisering og/eller inkorporering af EPC'er, der hæmmer dannelsen af nye blodkar og dermed også aktiviteten af de knogledannende celler. |
| Helingshastighed | Effektiv og robust heling med hurtig dannelse af callus og efterfølgende remodellering, der fører til fuld funktionsgenoprettelse inden for forventet tidsramme. | Forlænget helingsproces, øget risiko for forsinket heling (delayed union) eller manglende heling (non-union), hvor knoglen ikke vokser sammen. |
| Vævskvalitet | Dannelse af stærk og funktionel knogle, der kan modstå normal belastning. | Dannelse af svagere eller fibrøst væv i stedet for knogle, hvilket efterlader knoglen sårbar over for re-fraktur. |
Ofte Stillede Spørgsmål (FAQ)
For at opsummere og yderligere belyse emnet, her er svar på nogle ofte stillede spørgsmål:
Hvad er et knoglebrud?
Et knoglebrud er en fuldstændig eller delvis brud i kontinuiteten af en knogle. Det kan opstå som følge af traume, overbelastning eller underliggende sygdomme, der svækker knoglen, såsom osteoporose.
Hvorfor er blodkar så vigtige for knogleheling?
Blodkar er afgørende for knogleheling, fordi de leverer ilt og næringsstoffer til de helende celler og væv, samtidig med at de fjerner affaldsstoffer. Uden tilstrækkelig blodforsyning kan knoglen ikke reparere sig selv effektivt, hvilket fører til forsinket heling eller endda manglende heling.
Hvad er forskellen på vasculogenese og angiogenese?
Angiogenese er dannelsen af nye blodkar fra allerede eksisterende blodkar, typisk ved knopskydning. Vasculogenese er derimod dannelsen af nye blodkar de novo (fra bunden) fra forløberceller, som f.eks. EPC'er, der differentierer sig og samles for at danne nye rørformede strukturer. Begge processer er vigtige for at genoprette blodforsyningen efter en skade.
Kan man øge EPC-aktiviteten for at forbedre heling?
Dette er et aktivt forskningsområde. Selvom den foreliggende information ikke beskriver specifikke metoder, peger de på potentialet for terapeutiske interventioner. Det kunne potentielt indebære medicin, der stimulerer EPC-mobilisering, eller cellebaserede terapier, hvor EPC'er administreres direkte for at forbedre helingen. Mere forskning er nødvendig for at oversætte disse fund til klinisk praksis.
Hvordan ved forskere, hvor EPC'erne kommer fra?
Som beskrevet i artiklen, anvendte forskere avancerede teknikker som knoglemarvstransplantation fra transgene donorer (deres celler var mærket) og administration af celler mærket med Grønt Fluorescerende Protein (GFP). Disse metoder gjorde det muligt at spore cellernes oprindelse og destination, hvilket bekræftede, at de EPC'er, der bidrog til helingen på brudstedet, stammede specifikt fra knoglemarven.
Konklusion
Studiet af knoglemarvsafledte Endoteliale Forløberceller (EPC'er) har revolutioneret vores forståelse af knoglebrudsheling. Det er nu klart, at disse celler ikke blot er passive tilskuere, men snarere aktive deltagere i kroppens reparationsproces. Ved at mobilisere fra knoglemarven og rekrutteres til brudstedet spiller EPC'erne en essentiel rolle i at drive neovaskulariseringen, som er afgørende for en effektiv genopretning af blodforsyningen og dermed for den samlede helingssucces. Denne indsigt åbner spændende perspektiver for fremtidige behandlingsmetoder, der kan udnytte kroppens egne regenerative evner til at forbedre helingen af knoglebrud betydeligt.
Hvis du vil læse andre artikler, der ligner Knoglemarvens Mirakelceller: Heling af Brud, kan du besøge kategorien Teknologi.
